Krūts vēzis ir biežākais ļaundabīgais audzējs sievietēm. Latvijā ik gadu ar krūts vēzi saslimst aptuveni 1200 sievietes un tas ir viens no biežākajiem priekšlaicīgas nāves cēloņiem sievietēm vecumā virs 35 gadiem. Pasaulē un arī Latvijā ar krūts vēzi visbiežāk saslimst sievietes vecumā virs 50 gadiem. Taču Latvijā, tāpat kā citviet pasaulē, ik gadus saslimst arī jaunākas sievietes. Agrīnās slimības stadijās, krūts vēzi var veiksmīgi izārstēt, tāpēc īpaši svarīgi ir regulāri veikt krūts vēža skrīningu.
Katru gadu pasaulē saslimst ap 1 miljons sieviešu. Ik pēc 2 minūtēm Eiropas Savienībā kādai sievietei tiek diagnosticēts krūts vēzis, ik pēc 6 minūtēm kāda sieviete no tā mirst. Vēzis ir biežākais nāves cēlonis Eiropā. No krūts vēža katru gadu mirst 88 400 sieviešu un ap 1000 vīriešu.
Tā kā slimība ir bieži sastopama, tā ir arī daudz pētīta – meklēti tās cēloņi, attīstības mehānismi un ārstēšanas iespējas. Laika gaitā ir uzkrātas zināšanas, tiek apstiprināti arvien jauni medikamenti, līdz ar to pat izplatītas slimības gadījumos to ir iespējams sekmīgi ārstēt, pagarinot pacientes mūžu un nodrošinot labu dzīves kvalitāti.
Krūts vēzis ir audzējs, kas attīstās no krūtis veidojošiem audiem. Tas var attīstīties gan sievietēm, gan vīriešiem (tomēr vīriešiem sastopams ievērojami retāk). Audzēja attīstības pamatā ir krūtis veidojošo šūnu nekontrolēta augšana, dalīšanās un izplatība organismā.
Kopš 2009.gada Latvijā tiek īstenota valsts apmaksāta vēža savlaicīgas atklāšanas programma.
Sievietēm vecumā no 50 līdz 68 gadiem reizi divos gados uz deklarēto dzīvesvietas adresi tiek nosūtīta uzaicinājuma vēstule veikt valsts apmaksātu krūts vēža profilaktisko pārbaudi. Vēstule kalpo kā nosūtījums pārbaudes veikšanai. Profilaktisko pārbaudi var veikt arī tad, ja uzaicinājuma vēstule nav paņemta līdzi uz izmeklējumu (piemēram, ir nozaudēta vai nav saņemta). Informācija par uzaicinājuma vēstuli ārstniecības iestādēs pieejama elektroniski.
https://www.spkc.gov.lv/lv/veza-skrinings.
2023. gadā uzaicinājuma vēstuli krūts vēža profilaktiskās pārbaudes veikšanai saņems sievietes, kuras ir dzimušas 1955., 1957., 1959., 1961., 1963., 1965., 1967., 1969., 1971. un 1973. gadā. Uzaicinājums ir derīgs divus gadus, taču aicinām veikt izmeklējumu dažu mēnešu laikā no uzaicinājuma saņemšanas. Jāņem vērā, ka uzaicinājums netiek nosūtīts sievietei, kurai gada laikā līdz uzaicinājuma vēstules sagatavošanas datumam ir veikts mamogrāfijas izmeklējums.
Krūts dziedzera uzbūve
Divas galvenās krūts sastāvdaļas ir krūts dziedzeri un tos aptverošie taukaudi. Krūts dziedzeri veido 15-20 daivas, kas sastāv no mazākām daiviņām un vadiņiem. Katra daiviņa satur aptuveni 30 vadiņus (alveolas). Vadiņi pievienojas piena vadam, kas savienots ar krūtsgalu. Krūtsgalu aptverošo apvidu sauc par areolu. Areola ir pigmentēta, un uz to atveras arī daudz sīku tauku dziedzeru. Krūti balsta Kūpera saites un krūškurvja sienas muskuļi. Kūpera saites ir divi šķiedraudu slāņi, kas notur krūti pie krūškurvja. Vecums, aptaukošanās un vairākas grūtniecības izstaipa šīs saites, padarot krūti nokarenu un bez tvirtuma.
Hormonu svārstības menstruālā cikla laikā maina krūts fizioloģiju, šūnu līmenī sagatavojot piena dziedzeri zīdīšanai, ja iestājas grūtniecība. Ārēji šīs pārmaiņas izraisa krūšu palielināšanos vai mazināšanos, un tas ir atkarīgs no sievietes hormonu līmeņa.
Krūti ar asinīm apgādā paduses, starpribu un iekšējās krūškurvja artērijas. Tās aptver krūti virzienā no apvidus pie ādas virsmas uz dziedzera vidu. Līdzīgs asinsvadu tīkls ar dziļām un virspusējām vēnām aizvada asinis prom no krūts.
Krūtī ir daudz limfvadu. Mediālie jeb vidus limfvadi virzās uz iekšējiem krūts dziedzera limfmezgliem. Iekšējie limfvadi saplūst zematslēgas kaula limfmezglos un savienojas ar otras krūts limfmezgliem. Lielākā daļa šo vadu novietoti virzienā prom no krūtsgala.
Pirms pubertātes vīriešiem un sievietēm ir līdzīga krūts uzbūve. Taču sievietēm pubertātes laikā organismā strauji sāk izdalīties hormoni estrogēns un progesterons. Progesterona ietekmē veidojas daiviņas. Savukārt estrogēns stimulē pārmaiņas krūts audos, tāpēc:
· rodas papildu vadi;
· esošie vadi palielinās un veidojas jauna dziedzeru sistēma, kas spēj izdalīt pienu;
· saistaudi palielinās un kļūst vēl elastīgāki;
· palielinās taukaudu apjoms;
· palielinās asinsvadu daudzums.
Krūts parasti ir pilnīgi izveidojusies līdz 15 gadu vecumam. Šajā vecumā krūts audi ir palielinājušies izmēros un plešas horizontāli no krūšu kaula līdz padusei un vertikāli no otrās vai trešās ribas līdz sestajai vai septītajai ribai. Sievietes menstruālais cikls rada hormonu vidi, kas ilgstoši – līdz menopauzei – ietekmē krūts audus.
Grūtniecība un dzemdības izraisa hormonālas pārmaiņas, kas ļauj krūtij izdalīt pienu.
Krūts vēzis ir biežākais ļaundabīgais audzējs sievietēm. Ir aprēķināts, ka Eiropā ar krūts vēzi katra 8 - 9 sieviete.
Krūts vēzis ir biežāk sastopams gados vecākām sievietēm, tomēr 1 no 4 diagnosticētajiem gadījumiem ir sievietēm, kas jaunākas par 50 gadiem. Mazāk kā 5% krūts vēza gadījumu tiek noteikti sievietēm jaunākām par 35 gadiem.
Vairumā valstu mirstība no krūts vēža mazinās, uzlabojoties agrīnai diagnostikai un terapijas iespējām.
Krūts vēzis vīriešiem ir sastopams reti. Tikai aptuveni 1% no visiem krūts audzējiem tiek diagnosticēts vīriešiem (Pasaulē gada laikā slimo aptuveni 100 000 vīriešu).
Krūts vēza riska faktori
Krūts vēža attīstības iemesli nav precīzi zināmi. Literatūrā ir aprakstīta faktoru grupa, ko dēvē par – riska faktoriem. Tie ir faktori, kas palielina audzēja attīstības risku, tomēr ne visām sievietēm ar riska faktoriem attīstās audzējs un pretēji – pacientēm bez neviena no minētajiem riska faktoriem var attīstīties audzējs.
Galvenie riska faktori krūts vēza attīstībā:
Vecums – krūts vēza attīstības risks pieaug līdz ar pacientes vecumu;
Pārmantotas gēnu mutācijas – dažas no gēnu mutācijām var tikt pārmantotas no vecākiem, kas paaugstina krūts vēza attīstības risku. Šīs pārmantotās gēnu mutācijas sastopamas ap 10% krūts vēza pacientēm;
Ģimenes anamnēzē krūts vēzis un/vai olnīcu vēzis – krūts vēzis pirmās pakāpes radiniekiem (mātei, māsai, meitai, brālis, tēvam) īpaši, ja ģimenes locekļa vecums ir < 45 gadiem slimības diagnosticēšanas brīdī palielina krūts vēza attīstības risku. Ja vairākiem ģimenes locekļiem tiek diagnosticēts krūts un vai olnīcu vēzis, jāizvērtē ir pacientes ģenētiskās predispozīcijas iespējamība. Gēni – BRCA1 un BRCA2 ir divi biežākie, kuru mutācijas tiek pārmantotas ģimenes locekļiem. Saslimstības risks BRCA1 mutācijas nesējam (ja noteikta gēna mutācija) ir 80-85%, un 60 % gadījumu audzējs skar abas krūtis (bilaterāls audzējs). Šīm pacientēm būtu vēlama arī ārsta ģenētiķa un psihologa konsultācija, pirms plānotās operācijas, lai spētu izlemt par tās apjomu ar ķirurgu;
Krūts vēzis pacientes anamnēzē – palielina risku audzējam attīstīties tajā pašā krūtī vai otrā;
Laika periods, kad sievietes organismā tiek producēti estrogēni un progesterons, paaugstināts risks ir:
sievietēm, kurām menstruācijas sākās pirms 12 gadu vecuma un / vai menopauze iestājās pēc 55 gadu vecuma;
Labdabīgi krūts veidojumi, kas paaugstina audzēju attīstības risku: lobulāra carninoma in situ un atipiska duktāla hiperplāzija;
Staru terapija krūškurvja priekšējās sienas rajonam bērnībā / jaunībā (biežāk pacientēm, kurām ārstēta limfoma);
Blīva krūts dziedzera struktūra (dense breast)
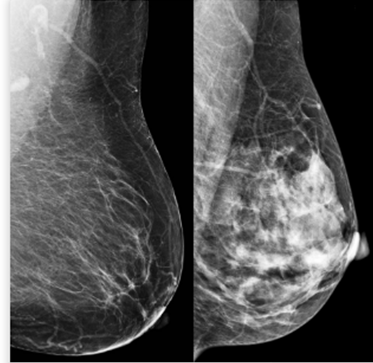
Bilde pa kreisi parāda taukainu krūts dziedzeri, bilde pa labi parāda blīvu krūts dziedzeri
Medikamenta Diethylstilbestrol lietošana. ASV 1940-1971 gadā šo medikamentu plaši lietoja grūtniecēm, lai novērstu spontāna aborta risku. Pašām sievietēm, kas lietoja šo medikamentu un arī viņu bērniem bija lielāks risks saslimt ar krūts vēzi.
Ietekmējamie riska faktori:
Sievietēm, kuras nav fiziski aktīvas ir lielāks risks uz krūts vēža attīstību
Liekais svars – liekais svars palielina krūts vēža attīstības risku, īpaši pēc menopauzes. Tas skaidrojams ar estrogēnu produkciju taukaudos, kas ir galvenais estrogēnu avots sievietes organismā laikā pēc menopauzes;
Alkohola lietošana un smēķēšana – risks pieaug pastāvot jebkuram no šiem faktoriem, tomēr iemesls tam nav skaidrs.
Estrogēnu vai progesteronu saturošu medikamentu lietošana:
perorālo kontraceptīvo līdzekļu lietošana īpaši pirms pirmās grūtniecības palielina krūts vēza attīstības risku. Laika periodam pēc pēdējās perorālo kontraceptīvo līdzekļu lietošanas sasniedzot 10 gadus – risks krūts vēza attīstībai ir tāds pats, kā pārējām sievietēm populācijā;
hormonus aizvietojošās terapija menopauzē palielina krūts vēza attīstības risku. Augstāks risks ir pacientēm, kas saņem kombinētu – estrogēnus un progesteronu saturošu terapiju, zemāks, ja pacientei nozīmēti tikai estrogēnus saturoši preparāti. Biežāk krūts vēzis attīstās pacientēm, kas lieto šo terapiju un neilgi pēc tās beigšanas. Pacientēm 5 gadus pēc hormonus aizvietojošas terapijas pārtraukšanas risks ir tāds pats, kā pārējām sievietēm populācijā;
· sievietes, kurām pirmais bērns dzimst pēc 30 gadu vecuma; nebarošana ar krūti, sievietes, kam grūtniecība nav bijusi pilna laika
· smēķēšana
Krūts vēža klasifikācijai tiek izmantota Tumor (audzēja), Node (limfmezglu), Metastases (metastāžu) jeb TNM sistēma.
Krūts vēža stadiju nosaka atbilstoši TNM klasifikācijai, pēc tam nosaka stadiju no 0 līdz IV balstoties uz AJCC (American Joint Committee on Caner) 8. izdevumu.
Pirmais faktors T audzēju klasifikācijā raksturo primārā audzēja izplatību.
T faktora pakāpes:
· T0 –Nav datu par primāru tumoru
· Tis – karcinoma in situ – duktāla karcinoma, daiviņu karcinoma in situ jeb neinvazīva; vai krūtsgala Pedžeta slimība bez audzēja.
· T1–nepārsniedz 2 cm lielākajā šķērsizmērā. ≤ 20 mm
· T1mi ≤ 1mm; T1a 1-5mm, T1b 5-10mm; T1c 10-20mm
· T2–lielāks par 2 cm, bet mazāks par 5 cm.
· T3–lielāks par 5 cm.
· T4–Cauraug krūškurvja sienu vai ādu.
· T4a invāzija krūškurvja sienā; T4b ādas izčūlojums/eritēma/tūska (neinflamators); T4c = T4a + T4b pazīmes; T4d inflamators vēzis*
· Tx- audzējs nav nosakāms
*Iekaisīgs jeb inflamators krūts vēzis sastāda 1-5% visu krūts vēžu. Atšķiras no klasiska krūts vēža ar to, ka no simptomiem prevalē iekaisuma aina – krūts pietūkums, apsārtums, āda kā “apelsīna miza”. Pacienti var nejust un nepalpēt veidojumu. Šis krūts vēža paveids biežāk attīstās jaunām sievietēm (< 40 g. v. ), ir pēc gaitas ļoti agresīvs (progresē nedēļu/mēnešu laikā), ātri metastazē. Diagnozes brīdī inflamators vēzis ir III vai IV stadijā. Var tikt sajaukts ar labdabīgu krūts iekaisumu (mastītu). Inflamatoram vēzim terapiju uzsāk ar pirmsoperācijas sistēmisku terapiju.
N liecina par limfmezglu metastāžu esamību un lokalizāciju. cN## klīniska stadija
· cNX–Nevar izmeklēt limfmezglus
· cN0– metastāžu limfmezglos nav.
· cN1 –metastāzes paduses limfmezglos tajā pašā pusē, kur audzējs; kustīgas. MTS ipsilaterālos I un II grupas paduses lmm, lmm nav fiksēti
· cN2–metastāzes paduses limfmezglos tajā pašā pusē, kur audzējs; fiksētas. MTS ipsilaterālos I un II grupas paduses lmm, kas ir fiksēti (cN2a) vai ipsilaterālos intermammāros lmm (cN2b)
· cN3 –metastāzes iekšējos krūts dziedzera limfmezglos tajā pašā pusē, kur audzējs. MTS ipsilaterālos infraklavikulāros (III gr) (cN3a); ipsilaterālos paduses un intermammāros lmm (cN3b); ipsilaterālos supraklavikulāros lmm (cN3c)
Limfmezgli (Patoloģisks) pN (operācijas materiāls)
· pNx* Nevar izmeklēt limfmezglus
· pN0 Nav datu par limfmezglu iesaisti
· pN1 MTS 1-3 paduses lmm (pN1a) vai intermammāros lmm, kas bija klīniski negatīvi (pN1b), vai abi kopā (pN1c); pN1mi = ja katra MTS ir 0.2-2mm liela
· pN2 MTS 4-9 paduses lmm (pN2a) vai intermammāros lmm, kas bija klīniski pozitīvi (pN2b)
· pN3 MTS 10+ paduses lmm vai infraklavikulāros lmm (pN3a); pN1a vai pN2a kopā ar pN2b (pN3b); pN2a + pN1b (pN3b); MTS supraklavikulāros lmm (pN3c)
*cNx un pNx piemēro, ja pacientei iepriekš veikta limfadenektomija un nav reģionālo limfmezglu vai arī operācijas laikā netika veikta reģionālo limfmezglu ekscīzija.
**Klīnisko N stadiju nosaka ar vizuāldiagnostikas metodēm, palpatori un ar limfmezglu aspirācijas citoloģiju (FNA), retos gadījumos ekscīzijas biopsiju.
M raksturo distālās mestastāzes.
· MX–distālas metastāzes nav vērtējamas.
· M0–distālu metastāžu nav.
· M1–ir distālas metastāzes, tostarp virsatslēgas kaula limfmezglos, tajā pašā pusē, kur audzējs.
Krūts vēža iedalījums pēc stadijas
Ikdienā pieņemts lietot vienkāršāku krūts vēža klasifikāciju – Starptautisko krūts vēža klasifikācijas sistēmu (ISS). Tā pilnībā balstās uz TNM klasifikācijas datiem, bet tiek grupēta stadijās:
|
TNM apraksts |
Stadija |
|
Tis (in situ) |
0 |
|
T1 N0 M0 |
IA |
|
T0N1miMo T1N1miMo |
IB |
|
T0 N1 M0 |
IIA |
|
T2 N0 M0 |
IIA |
|
T1N1Mo |
IIA |
|
T2 N1 M0 |
IIB |
|
T3 N0 M0 |
IIB |
|
T0 N2 M0 |
IIIA |
|
T1 N2 M0 |
IIIA |
|
T2 N2 M0 |
IIIA |
|
T3 N1 vai N2 M0 |
IIIA |
|
T4 N0 M0 |
IIIB |
|
T4 N1 M0 |
IIIB |
|
T4N2Mo |
IIIC |
|
T jebkurš N3 |
IIIC |
|
Jebkurš T jebkurš N M1 |
IV |
Lai varētu spriest par piemērotāko ārstēšanu, noteikti jāņem vērā visi faktori – audzēja stadija, veids, receptoru statuss. Tomēr viennozīmīgi ir skaidrs, ka pēc iespējas agrīnāka vēža diagnostika palielina cerību izārstēties.
Gēni, kas nosaka krūts vēža attīstību
Tāpat kā vairākumā vēža gadījumu, arī krūts vēža attīstībā nozīme ir specifiskiem gēniem.
BRCA1
Par BRCA1 gēna mutācijām pirmo reizi tika ziņots 1994. gadā. Šis gēns atrodas 17. hromosomas garajā plecā (17q21) un piedalās DNS pārrāvumu labošanā. Tomēr mutācijas BRCA1 neļauj šo labošanu veikt, tāpēc rodas vairāk DNS replikācijas kļūdu un vēzis aug intensīvāk. BRCA1 mutācijas vecumā līdz 45 gadiem palielina krūts vēža risku par aptuveni 50%, bet visas dzīves laikā – par 85%. Sievietēm ar BRCA1 gēna mutāciju krūts vēzis bieži rodas agrāk nekā vispārējā populācijā.
BRCA2
BRCA2, kas lokalizēts 13. hromosomā, saistīts ar agrīnu krūts vēža rašanos un kopumā palielina krūts vēža risku gan sievietēm, gan vīriešiem. BRCA2 izdalīšanās palielinās strauji dalošās šūnās un diferencējošās krūts dziedzera epitēlija šūnās kā atbildes reakcija uz noteikta veida hormoniem – glikokortikoīdiem. BRCA2 mutāciju radītais krūts vēža risks ir līdzīgs tam, ko rada BRCA1.
p53
Audzēju nomācošais proteīns p53 novērš bojātās DNS replikāciju normālās šūnās. Bojātas p53 molekulas ļauj izdzīvot šūnām, kurās ir bojāta DNS; bojātā DNS dalīšanās procesā tiek nodota meitšūnām, kurās pievienojas vēl citas mutācijas, un rezultātā attīstās audzēji. Diemžēl veselo šūnu sargājošais gēns p53 ir bijis bojāts apmēram pusei cilvēku, kam konstatēts audzējs.
ATM
Ataksijas-teleangiektāzijas mutantais (ATM) gēns palielina krūts vēža rašanās risku. Lai gan ATM gēna darbības mehānisms vēl nav pilnīgi noskaidrots, normāli tam ir nozīmīga loma bojātas DNS labošanā.
PIK3CA- Gēns satur norādījumus proteīna p110 alfa (p110α) ražošanai. P110α organismā veic daudzas funkcijas, tostarp: šūnu augšana un dalīšanās, šūnu kustība, olbaltumvielu ražošana, vielu transportēšana šūnās, šūnu izdzīvošana. PI3K signalizācija var būt iesaistīta arī dažu hormonu regulēšanā. Gēnu mutācija var izjaukt šo procesu, izraisot nekontrolētu šūnu dalīšanos un replikāciju. Tas veicina daudzu vēža veidu attīstību, tostarp:
krūts vēzis
olnīcu vēzis
resnās zarnas vēzis
smadzeņu vēzis
mutācijas tiek konstatētas 40 procentiem estrogēnu receptoru (ER) pozitīvo un epidermas augšanas faktora receptoru 2 (HER2) negatīvo krūts vēža gadījumu.
CHEK2 gēns lokalizēts 22 hromosomas 11 pozīcijā. o CHEK2 gēns sintezē proteīnkināzi, kura darbojas k darbojas kā audzēju nomācēja regul , regulē šūnu dalīšanos un augšanu. 1000delC- saistāma ar krūts vēzi.
Pašlaik šo gēnu noteikšana ir vairāk zinātniska nekā praktiska. Tomēr nākotnē onkoloģijas uzdevums un mērķis ir ar gēnu inženierijas palīdzību „izlabot” mainītos gēnus un novērst vēža rašanās iespēju.
Krūts vēža klasifikācija
0 stadija:
audzēja pirmsākums. Lai arī pagaidām nekas vēl neliecina par vēža šūnu negatīvo ietekmi uz veselību, rentgenoloģiski tas jau ir saredzams.
I stadija:
krūts vēzis ir sācis attīstīties. Audzējs (veidojums krūtī) ir samērā neliels – līdz 2 cm diametrā. Izteikti palielināti limfmezgli parasti netiek novēroti. Krūts vēzis, kas atklāts I stadijā, 90% gadījumu ir pilnībā izārstējams.
II stadija:
audzēja izmērs ir 2-5 cm diametrā. Ja tas ir mazāks par 2 cm diametrā un ja arī audzēja skartās puses rokas padusē parādās palielināti limfmezgli, tas ir pieskaitāms otrajai stadijai.
III stadija:
audzējs nereti pārsniedz 5 cm diametrā, taču var būt arī mazāks. Krūts vēzi III stadijā raksturo:
· vairāki palielināti limfmezgli ne tikai padusē, bet arī citos tuvākajos audos;
· krūts vēzis sācis bojāt arī citas organisma struktūras – krūts ādu, krūškurvja sienu vai iekšējos piena dziedzeru limfmezglus.
IV stadija:
krūts vēzis ir izplatījies arī uz citiem iekšējiem orgāniem (plaušām, kauliem u. c.).
Metastāzes
Krūts vēzis var izplatīties jeb metastazēties vietējas, reģionālas vai attālas jeb distālas diseminācijas veidā.
Vietēja diseminācija nozīmē, ka vēža šūnas „aizķeras” turpat netālu no primārā jeb sākotnējā audzēja; visbiežāk tās ir krūškurvja sienas struktūras, piemēram, pleca pinums, ribas, pleira. Šāda diseminācija nereti nonāk līdz ādas virsmai.
Ar limfātiskās sistēmas starpniecību vēzis var izplatīties krūts dziedzeru iekšējos, virsatslēgas vai sānu grupas limfmezglos, radot reģionālas metastāzes.
Distālas jeb attālas, ar asinīm pārnestas metastāzes galvenokārt rodas kaulos, aknās, plaušās, ādā un centrālajā nervu sistēmā gan galvas, gan muguras smadzenēs. Izplatīšanās ar asinīm ir bīstama, jo bieži tieši attālās metastāzes ir nāves cēlonis.
Kaulu bojājumi
Kaulu sāpes pacientiem ar vēzi parasti izraisa vēža šūnas, kas iekļuvušas kaulos, – tās sauc par kaulu metastāzēm. Kaulu sāpes bieži ir pirmais kaulu metastāžu simptoms, kāpēc tiek veiktas pārbaudes, kas apstiprina šo diagnozi. Kaulu bojājumu ārstēšana ir vērsta uz sāpju mazināšanu, lūzumu riska mazināšanu, lūzumu ārstēšanu un papildu kaulu komplikāciju novēršanu vai aizkavēšanu.
Kas izraisa kaulu sāpes?
Bieži sastopams kaulu sāpju cēlonis ir metastātisks vēzis. Vēža izplatīšanos no tā sākotnējās vietas uz citu vietu ķermenī sauc par metastāzēm. Kaulu metastāzes nav jauns vai cits vēzis – tas sastāv no vēža šūnām no sākotnējā vēža, piemēram, krūts, priekšdziedzera, plaušu, nieru vai vairogdziedzera vēža šūnas, kas izplatījušās kaulos.
Vēža šūnas var izplatīties jeb metastazēties visā organismā un limfātiskajā sistēmā. Kauli ir vieta ķermenī, kur vēzis metastazējas visbiežāk. Kaulos metastāzes parasti nokļūst ar asinsrites palīdzību. Vēža šūnas atdalās no sākotnējās vietas organismā un ceļo pa asinsvadiem, līdz nostiprinās pie asinsvada sienas mazā kapilāru tīklā kaulaudos. Vēzis var nonākt kaulos arī ar tiešu ieaugšanu no blakus vēža, lai gan tas notiek retāk nekā izplatīšanās ar asinsriti.
Sāpes kaulu vēža gadījumā rodas tāpēc, ka vēzis izjauc normālo šūnu darbības līdzsvaru kaulos, izraisot kaulaudu struktūras izmaiņas. Vesels kauls tiek nepārtraukti remodelēts jeb notiek kaulaudu sabrukšana un atjaunošanās. Vēža šūnas, kas izplatījušās kaulos, izjauc šo līdzsvaru starp osteoklastu (šūnu, kas sadala kaulus) un osteoblastu (šūnu, kas veido jaunu kaulu) darbību, izraisot pavājinātu vai pastiprinātu kaulu veidošanos. Šie traucējumi var skart vai nu periostu (bieza membrāna, kas klāj kaulu, saukta arī par kaula plēvi), vai arī stimulēt nervus kaulā, izraisot sāpes.
Kā diagnosticē kaulu metastāzes?
Kaulu metastāzes parasti tiek diagnosticētas, meklējot iemeslu sāpēm kaulos. Tiek veikta rentgena caurskate vai sarežģītāka procedūra, ko sauc par kaulu skenēšanu, lai noskaidrotu, vai sāpes izraisa ar vēzi saistīts kaulu bojājums. Kaulu skenēšanas laikā vēnā tiek ievadītas zema līmeņa radioaktīvas daļiņas. Tās cirkulē pa visu organismu un nokļūst arī kaulos. Liela šo radioaktīvo daļiņu koncentrācija kaulu skenēšanas attēlā liecina par vēža šūnu klātbūtni.
Kaulu sāpes var būt grūti atšķiramas no parastām muguras sāpēm vai artrīta. Parasti kaulu metastāžu izraisītas sāpes ir diezgan pastāvīgas, arī naktī. Tās var pastiprināties dažādās pozās, piemēram, stāvot (ja vēža šūnas ir svaru nesošajā kaulā). Ja sāpes ilgst nedēļu vai divas un šķiet, ka nemazinās un neatgādina citas pārciestas sāpes, noteikti jākonsultējas ar ārstu.
Kaulu metastāzes parasti ir skeleta centrālajā daļā, lai gan tās var būt jebkurā vietā kaulu sistēmā. Bieži kaulu metastāzes atrod mugurkaulā, iegurnī, augšstilbā, ribās, augšdelmā un galvaskausā; šajās vietās atklāj vairāk nekā 90% visu kaulu metastāžu.
Kā ārstē kaulu sāpes?
Kaulu metastāžu izraisītu kaulu sāpju ārstēšanas mērķis ir mazināt sāpes, ārstēt lūzumus, mazināt lūzumu risku un novērst vai aizkavēt citu komplikāciju rašanos. Kaulu metastāžu ārstēšanas paņēmieni – pretsāpju zāles, bisfosfonāti, staru terapija un/vai ķirurģiska ārstēšana.
Pretsāpju medikamenti
Vēža izraisītas kaulu sāpes var ārstēt ar dažādām pretsāpju zālēm. Lai gan 90% vēža slimnieku sāpes izdodas mazināt, nekontrolējamas, ar vēzi saistītas sāpes joprojām ir problēma, īpaši pacientiem, kas dzīvo mājās.
Pasaules Veselības organizācijas (PVO) vēža sāpju mazināšanas ieteikumi norāda, ka pacientu sāpju stiprums, kas tiek vērtēts pēc 1-10 punktu skalas, nosaka, kādu pretsāpju zāļu veidu izvēlēties.
· Vieglas vai vidēji stipras sāpes (1-3 punkti): neopioīdi ir pirmās izvēles ārstēšanas līdzekļi vieglu vai vidēji stipru sāpju gadījumā. Pie šīs zāļu grupas pieder, piemēram, paracetamols, un nesteroīdie pretiekaisuma līdzekļi (NPL), piemēram, ibuprofēns.
· Vidēji stipras vai stipras sāpes (4-6 punkti): pacientiem ar vidēji stiprām vai stiprām sāpēm, kuriem pirmā līmeņa ārstēšana nav palīdzējusi, jāsaņem pretsāpju līdzekļi, kas pieder opioīdu klasei, t. i., narkotiskie analgētiskie līdzekļi. Šīs klases medikamentus var iegādāties tikai ar ārsta recepti. Var pievienot acetaminofēnu vai NPL.
· Stipras sāpes (7-10 punkti): pacientiem ar stiprām sāpēm, kā arī pacientiem, kam sāpes nav mazinājusi iepriekšējā ārstēšana, jānozīmē spēcīgāks opioīdu līdzeklis (tā iegādei nepieciešama īpašas uzskaites recepte). Dažos gadījumos, iespējams, jāpievieno neopioīdu klases medikamenti, piemēram, aspirīns, paracetamols, ibuprofēns un citi pretsāpju terapijas pastiprinātājlīdzekļi.
Pretsāpju zālēm var būt blakusparādības – miegainība, aizcietējums, reibonis, slikta dūša un vemšana. Atvieglojums no pretsāpju zālēm ir īslaicīgs, un sāpes drīz var atsākties, tāpēc medikamentus vislabāk lietot tūlīt pēc sāpju sākšanās vai arī regulāri.
Bisfosfonāti
Medikamentu grupa bisfosfonāti var efektīvi mazināt kaulaudu zudumu, kas rodas no metastātiskiem bojājumiem, mazināt lūzumu risku un sāpes. Bisfosfonāti darbojas, nomācot kaulu rezorbciju jeb sabrukšanu. Kaulaudus nepārtraukti ietekmē divu veidu šūnas: osteoklasti, kas noārda vecās kaulaudu šūnas, un osteoblasti, kas atjauno. Savukārt vēža šūnas izdala dažādus faktorus, kas stimulē osteoklastu aktivitāti. Lai gan precīzs bisfosfonātu darbības mehānisms nav skaidrs, uzskata, ka tie kavē un iznīcina noārdošās šūnas osteoklastus, tādējādi mazinot kaulaudu sairšanu. Vairāk nekā 30 klīnisko pētījumu dati liecina, ka pacientiem ar kaulu metastāzēm, kuri tika ārstēti ar bisfosfonātiem, pagāja lielāks laika posms līdz kaulu lūzumiem, bija mazāka nepieciešamība pēc staru terapijas, mazinājās hiperkalciēmija (paaugstināts kalcija līmenis asinīs) un mazinājās nepieciešamība pēc ortopēdiskas ķirurģiskas operācijas.
Klīniskajos pētījumos pierādīts, ka bisfosfonāti novērš vai aizkavē kaulu sabrukšanu un ar to saistītās sāpes pacientiem, kam bija kaulu metastāzes no:
· krūts vēža;
· priekšdziedzera vēža;
· plaušu vēža;
· multiplās mielomas;
· nieru šūnu karcinomas.
Staru terapija
Staru terapija efektīvi mazina kaulu sāpes un vēža izplatīšanos kaulos. To pielieto gadījumos, kad nav tūlītēja lūzuma riska. Staru terapija ir īpaši efektīva, kad metastātiskie bojājumi ir tikai kādā vienā apvidū.
Vienu no staru terapijas veidiem sauc par radio-medikamentozo terapiju. Tas ietver radioaktīvas vielas, piemēram, stroncija-89, injekciju vēnā. Šī viela piesaistās tiem kaulu apvidiem, kuros ir vēzis. Šādā veidā novirzot starojumu tieši uz bojātiem kaulu rajoniem, tiek iznīcinātas aktīvās vēža šūnas kaulā un mazinās simptomi (sāpes). Iespējamās radio-medikamentozās terapijas blakusparādības ir samazināts asins šūnu skaits (palielināts asiņošanas risks) un, retos gadījumos, leikozes risks.
Ķirurģiska ārstēšana
Ķirurģiska operācija ir nepieciešama tūlītēja lūzuma riska gadījumā vai arī tādēļ, lai stabilizētu novājināto kaulu. Lai stiprinātu metastāzes bojāto kaulu vai izveidotu tā struktūru, ķirurģiski kaulā var ievietot metāla stieņus, plāksnītes, skrūves u. c.
Krūts vēža biežākie simptomi ir sāpes un diskomforts. Ne vienmēr visām sievietēm tas izpaužas ar veidojumu krūtī.
Ļaundabīga krūts audzēja pazīmes var būt šādas:
· bumbulis vai sabiezējums krūtī;
· palielināti limfmezgli padusē;
· izmaiņas krūts izmērā vai krāsā;
· krūtsgala jutīgums vai sāpes;
· brūngani vai asiņaini izdalījumi no krūtsgala vai tā ieraušanās uz iekšu;
· krūts ādas vai krūtsgala apsārtums, zvīņainums, nieze;
· krūts ādas krokojums vai iedobums tajā;
· tīklojums, kas ir redzamāks nekā parasti;
· savāds jutīgums, īpaši, ja tas ir tikai vienā krūtī.
Atcerieties! Parasti izrādās, ka šo simptomu iemesls nav krūts vēzis, bet tie noteikti liecina, ka jums jādodas pie ginekologa, ģimenes ārsta vai onkologa. Lūdzu, nebaidieties no onkologa pieminēšanas – Latvijā krūts slimības (arī labdabīgas pārmaiņas) tradicionāli ir onkologa (ķirurga mammologa) pārraudzībā.
Iemesli, kādēļ rodas aizdomas par krūts vēzi var būt dažādi: atradne skrīninga mamogrāfijas izmeklējumā, krūts palpatoras (krūtis izmeklē ar rokām pati paciente vai ārsts) izmeklēšanas laikā sataustīts veidojums, krūts ādas pārmaiņas, izdalījumi no krūts gala vai tā izskata / formas izmaiņas.
Diagnozes noteikšana ietver:
klīniskā izmeklēšana – tiek izmeklētas krūtis un reģionālie (tuvumā esošie) limfmezgli;
Radioloģiskā izmeklēšana – atkarībā no pacientes vecuma un krūšu blīvuma īpatnībām ārsts izvēlēsies papildus vizuālās diagnostikas izmeklējumus: mamogrāfiju (krūts rentgenoloģisku izmeklējumu), ultrasonoskopiju vai kombinēs abas metodes, lai iegūtu precīzus datus par veidojumu krūtī un reģionāliem limfmezgliem.
Atsevišķām pacientēm (īpaši gados jaunām, ar blīvām krūtīm, sievietēm ar zināmu BRCA gēna mutāciju vai krūts implantiem, plānā- krūts saaudzējoša operācija) papildus nepieciešams magnētiskās rezonanses izmeklējums krūtīm.
Lai izslēgtu audzēja izplatību (attālas metastāzes) tiek nozīmēti papildus izmeklējumi: dažos gadījumos plaušu rentgenogramma, vēdera dobuma ultrasonogrāfija, datortomogrāfija krūšu kurvim, vēdera dobumam, PET-CT, un skeleta scintigrāfija;
audu parauga histoloģiskā izmeklēšana – audu paraugs, kas tiek iegūts biopsijas vai operācijas laikā tiek izmeklēts zem mikroskopa. Šis ir galvenais izmeklējums, kas nosaka – vai veidojums ir labdabīgs, vai ļaundabīgs. Papildus tiek aprakstīti citi terapijas metodes izvēlei nozīmīgi audzēja raksturlielumi.
Izmeklēšanas metodes
Lai uzlabotu krūts vēža prognozi, vissvarīgākā ir agrīna diagnostika. Tas nozīmē, ka jāatklāj pēc iespējas mazi audzēji, pirms tie izplatās uz limfmezgliem.
Sievietēm, sākot no pilngadības vecuma, regulāri ir jāveic krūts dziedzeru kontrole. Pašpārbaudes mērķis ir sievietei pierast pie savu krūšu struktūras – tā savlaicīgi atklājot izmaiņas. Jo ātrāk tās konstatētas, jo sekmīgāki tālākie ārstēšanas rezultāti.
Nelielus audzējus iespējams noteikt ar attēldiagnostikas mamogrāfijas palīdzību. Mamogrāfiski noteikts audzējs izskatīsies kā neregulāras formas apvidus, kurā redzami smalki kaļķa izgulsnējumi jeb kalcifikācija.
Lai apstiprinātu krūts vēža diagnozi, ir svarīgi izmantot arī citas metodes – svārpsta biopsiju, ekscīzijas biopsiju, aspirācijas citoloģiju un aspirāciju ar tievu adatu.
Noderīgs būs arī slimnieka vai viņa tuvinieku stāstījums par slimības sākumu un attīstības gaitu, kas dod ārstam nepieciešamās ziņas diagnozes noteikšanai.
· Krūšu pašizmeklēšana
Ikmēneša krūšu pašizmeklēšana ir visām sievietēm pieejama metode, kas palīdz laikus atklāt brīdi, kad būtu nepieciešams doties pie ārsta. Krūšu pašizmeklēšana ir jāveic visām sievietēm reproduktīvā vecumā 1x mēnesī, iztaustot abus krūts dziedzerus visos četros kvadrantos.
Kad?
Jāizvēlas laiks, kad krūtis nav īpaši jutīgas. Sievietēm, kam ir regulāras menstruācijas, to iesaka veikt nedēļu pēc menstruāciju sākšanās. Sievietēm, kam jau vismaz gadu ir menopauze vai ir izoperēta dzemde un olnīcas – jebkurā pašu izraudzītā noteiktā dienā. Sievietēm, kas lieto hormonālās kontracepcijas tabletes, – katra jaunā iepakojuma pirmās tabletes ieņemšanas dienā.
Cik bieži?
Pārmaiņu atklāšanai ir būtiski, lai krūtis izmeklētu ne retāk kā reizi mēnesī.
Kā?
Adaptēts no: Walker HK, Hall WD, Hurst JW, editors. Clinical Methods: The History, Physical, and Laboratory Examinations. 3rd edition. Boston: Butterworths; 1990. Available from: https://www.ncbi.nlm.nih.gov/books/NBK201/
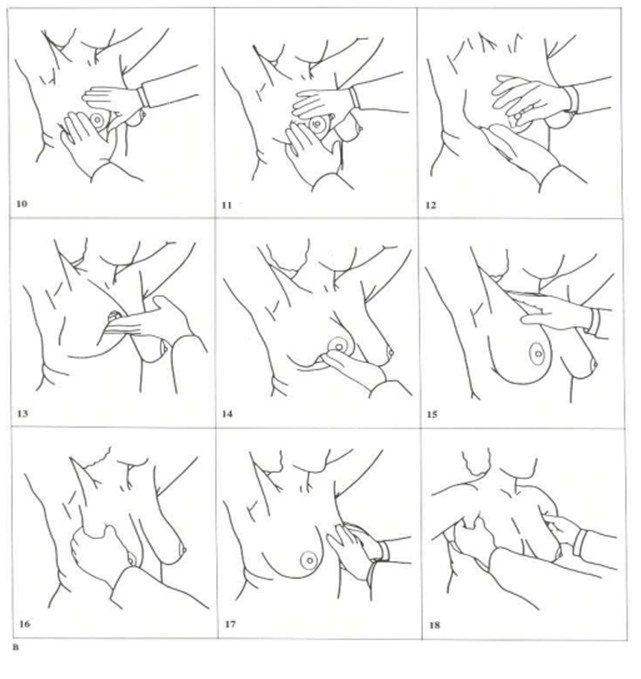
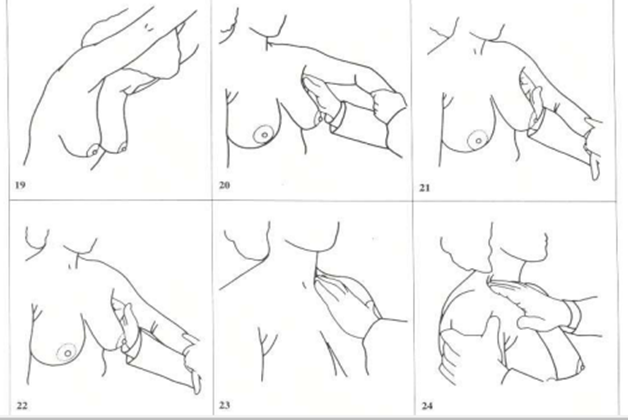
1. solis. Apskate. Nostājieties spoguļa priekšā un labā apgaismojumā aplūkojiet savas krūtis. Nolaidiet rokas gar sāniem, uzmanīgi aplūkojiet un salīdziniet abas krūtis. Pievērsiet uzmanību, vai nav manāmas izmaiņas krāsā, formā un lielumā, vai nav parādījies asimetrisks pastiprināts vēnu zīmējums, vai nav parādījušies neparasti ādas bojājumi – apsārtumi, sabiezējumi, mezgliņi, čūliņas. Uzmanība jāpievērš krūšu galiem, vai tie nav ievilkti uz iekšu, vai uz tiem nav izsitumu.
2. solis. Paceliet rokas virs galvas un apskatiet krūtis vēlreiz – vai arī šādā pozīcijā krūtis nav deformētas, neparādās neparasti izvirzījumi, vai abi krūtsgali atrodas vienādā augstumā un nav kā citādi mainījušies.
3. solis. Iztaustiet krūtis, kā arī paduses un kakla sānu daļas. To visērtāk izdarīt, ja iztaustāmās puses roku iespiedīsiet sānos, tādējādi sasprindzinot krūškurvja muskuļus, vai ļausiet tai brīvi nokarāties. Ar otras rokas iztaisnotiem, kopā saliktiem pirkstiem rūpīgi apļveidā iztaustiet visu krūti no augšas uz leju, no krūts malām uz centru un atpakaļ. Sāciet katru krūts daļu izmeklēt ar maigāku pieskārienu un tad palieliniet spiedienu, lai sajustu audu dziļākos slāņus. Kad trīs pirksti pietiekami piespiesti krūtij, veiciet divas trīs apļveida kustības, tad pirkstus atlaidiet un pārvietojiet uz nākamo vietu.
4. solis. Krūtsgali. Maigi saspiediet krūtsgalu starp rādītājpirkstu un īkšķi, vērojiet, vai nav izdalījumu, īpaši, vai tas nav dzeltenīgs šķidrums. Taustot neaizmirstiet arī apvidu zem paša krūtsgala!
5. solis. Pārbaude guļus stāvoklī. Varat to darīt gultā pirms iemigšanas vai pēc pamošanās. Pārbaudot labo krūti, novietojiet spilvenu zem labā pleca, labo roku aizliekot aiz galvas. Pievērsiet uzmanību veidojumiem un sacietējumiem. Tāpat izmeklējiet kreiso krūti.
Atcerieties!
Ja jums šķiet, ka neprotat izmeklēt savas krūtis pietiekami labi, jums ir tiesības lūgt ārstu izmeklēt krūtis un parādīt, kā to pareizi darīt.
Īss video- kā veikt pašpalpāciju – skatīt šeit.
· Mamogrāfija
Mamogrāfija ir krūts audu rentgenoloģiska izmeklēšana ar zemas intensitātes rentgenstarojumu. Šī uzskatāma par vienu no efektīvākajām metodēm, lai savlaicīgi atklātu krūts vēzi.
Pārbaudes laikā krūts tiek saspiesta, lai labāk būtu iespējams uzņemt rentgena attēlu. Mamogrāfijas metode var radīt nekomfortablas sajūtas, jūtīgākas sievietes to var uztvert kā nelielas sāpes. Rentgena attēla uzņemšana ilgst 2 minūtes, bet viss apmeklējums – apmēram 20 minūtes.
No 2012.gada augusta mēneša Latvijā ir pieejama jauna padziļināta krūts izmeklēšanas metode - mamogrāfija ar tomosintēzi. Viena izmeklējuma laikā tiek veikti divi izmeklējumi – digitālā mammogrāfija un padziļināta izmeklēšana, ko nodrošina tomosintēze. Tomosintēze - attēlveidošanas tehnoloģija, ar kuras palīdzību iegūst krūts izmeklējumus trīs dimensiju attēlos, kuri veidojas no dažādiem projekcijas leņķiem. Attēla projekcija tiek rekonstruēta, krūti šķērsgriezumā attēlojot ar soli ik pa 1 mm. Šī izmeklējuma metode ir ievērojami precīzāka, var agrīnāk atklāt izmaiņas un iespējamo pataloģiju, jo speciālistiem ir iespēja attēlu aplūkot slāni pa slānim, redzēt struktūras katrā slānī atsevišķi un aplūkot kustīgu attēlu no 3 pusēm. Vairāk informācijas par šo metodi lasiet šeit vai www.mamografija.lv
Pirmoreiz mamogrāfiju vēlams veikt 40 gadu vecumā.
Visām 50-69 gadus vecām sievietēm reizi divos gados valsts apmaksā mamogrāfijas izmeklējumu. Ja saņemat Nacionāla veselības dieniesta (NVD) izsūto uzaicinājuma vēstuli mamogrāfijas izmeklējumu veikšanai, lūdzu to rūpīgi izlasiet un izmantojiet šo iespēju veikt pārbaudi par valsts budžeta līdzekļiem.
Mamogrāfijas rezultāta koda skaidrojums
R1 – norma
R2 – potenciāli labdabīga atrade/atsevišķs labdabīgs veidojums
R3 – aizdomas par patoloģiju/lokālas patoloģiskas izmaiņas
R4 – potenciāla malignitāte/aizdomas par ļaundabīgu veidojumu
R5 – pierādīta malignitāte /ļaundabīga atrade
· R0 Rezultāts nav interpretējams
· R1 Norma; turpina piedalīties organizētajā skrīningā ik pēc 2 gadiem
· R2 Tipiski labdabīgas pazīmes; turpina piedalīties organizētajā skrīningā ik pēc 2 gadiem
· R3 Drīzāk labdabīgas pazīmes; var būt nepieciešama papildus izmeklēšana
· R4 Aizdomīga pazīmes; indicēta biopsija
· R5 Pārliecinošas ļaundabīguma pazīmes; indicēta biopsija vai operācija
Avots: http://www.vmnvd.gov.lv
Vairāk informācijas par mamogrāfiju – www.mamografija.lv
Vairāk informācijas par valsts apmaksāto profilaktisko apskašu programmu - www.vmnvd.gov.lv
Anamnēze
· Ģimenes onkoloģiskā anamnēze – mērķtiecīgi jājautā pacientei par krūts, olnīcu vēža gadījumiem ģimenē vairākās paaudzēs, par citām onkoloģiskās slimībām ģimenē. Ja ģimenē ir izsekojami vairāki krūts vēža un/vai olnīcu vēža gadījumi, tad tiek apsvērta ģenētisko mutāciju noteikšana. Krūts vēža gadījumā Latvijā nosaka BRCA1 gēna mutācijas pacienta asinīs (skat. BRCA mutāciju tests).
· Pacientes onkoloģiskā anamnēze – vai iepriekš ir bijušas onkoloģiskas saslimšanas un kāda bija saņemtā ārstēšana
· Reproduktīvā anamnēze – vai ir regulārs menstruālais cikls, menopauze, premenopauze. Kāda ir grūtniecību un dzemdību anamnēze.
· Medikamentoza anamnēze – vai paciente lieto hormonālo kontracepciju (Hormonaizvietojošā terapijas, HAT). HAT ilgstoša lietošana paaugstina krūts vēža attīstības risku.
Citi izmeklējumi Vizuāldiagnostikas izmeklējumi
· Krūts dziedzera ultrasonogrāfiskas izmeklēšanas metode ļauj atšķirt audzēju no piena dziedzera cistas. Izmeklējums parasti veicams pēc MG, atradnes precizēšanai, atsevišķos gadījumos aizvieto MG (piem., pacientēm ar krūšu implantiem). Slēdziens tiek klasificēts pēc BIRADS sistēmas, kur BIRADS 1 – pārliecinoši labdabīgas pārmaiņas un BIRADS 5 ir pārliecinoši ļaundabīgas. USG speciālists izmeklējuma laikā var paņemt krūšu dziedzera audu biopsiju, paduses limfmezglu tievās adatas aspirācijas biopsiju (citoloģiju), ja pastāv aizdomas par malignitāti. Uz izmeklējumu var nosūtīt gan ģimenes ārsts, gan mammologs.
· Sonoelastogrāfija - neinvazīva un nesāpīga krūšu izmeklēšanas metode, kas izstrādāta, pamatojoties uz mīksto audu ultrasonogrāfisko izmeklēšanu. Elastogrāfijas procesā uz audiem iedarbojas ar paaugstinātu spiedienu. Šī metode papildina ultraskaņas izmeklējumu ar speciālu programmu, kas spēj noteikt atšķirīgus elasticitātes modeļus konkrētai audu grupai, bet nespēj aizvietot mamogrāfiju. Ar šo metodi iespējams precīzāk noteikt veidojuma raksturu un atklāt vēži tā agrīnas stadijās.
· Krūškurvja rentgenā noskaidro audzēja izraisītos procesus plaušu audos.
· Skeleta skenēšana sniedz informāciju par audzēja skarto kaulu stāvokli. Šā izmeklējuma laikā pacients saņem nelielu apstarojuma devu, taču atklātie perēkļi var būt arī infekcijas sekas.
· Datortomogrāfija (CT) ir rentgenoloģisks izmeklējums, kura laikā tiek izdarīti vairāki rentgena uzņēmumi no dažādiem leņķiem, un tas ļauj izveidot detalizētu iekšējo orgānu ainu un ieraudzīt bojājumus.
· Magnētiskā rezonanse (MRI) ir metode, kas izmanto radioviļņu un magnētiskā lauka īpašības. Šo metodi izvēlas krūts dziedzera, galvas un muguras smadzeņu izmeklēšanai. Tiek veikta atsevišķos gadījumos kā papildus izmeklējums un biežāk tiek veikta jau tad, kad krūts vēža diagnoze apstiprināta histoloģiski. Indikācijas: jaunām sievietēm ar blīvu krūšu parenhīmu; ja tiek plānota neoadjuvanta terapija; ja 9 mammogrāfijas un ultrasonogrāfijas atradne nav pietiekami precīza; ja audzējs ir multifokāls; ja biopsijas atradne neatbilst klīniskiem datiem. Izmeklējumu nozīmē mammologs (ķirurgs, kas specializējas krūšu slimībās). Krūšu dziedzeru magnētiska rezonanse tiek veikta specializētos centros, kur strādā radiologi ar specializāciju krūšu dziedzeru patoloģijā (P. Stradiņa KUS, RAKUS LOC, ARS).
· Pozitrona emisijas tomogrāfijas (PET) izmeklēšanā tiek izmantota īpaša radioaktīva viela. Vēža šūnas uzņem šo vielu, un speciālas ierīces šīs šūnas atpazīst. Šo metodi izmanto, ja ir aizdomas par vēža izplatību, kā arī izmeklējot limfātiskos mezglus pirms to izgriešanas.
Pēc vēža atklāšanas tiek veikta papildu izmeklēšana terapijas precizēšanai.
Krūts dziedzera biopsija
a. Parasti tiek veikta Core, jeb audzēja “serdes” biopsija USG kontrolē ar speciālu adatu. To dara mammologs vai diagnostiskais radiologs ar specializāciju krūts ultrasonogrāfijā un biopsijā. Ja patoloģija ir saskatāma tikai MG, Core biopsiju veic MG kontrolē. Procedūru veic lokālā zemādas infiltrācijas anestēzijā ar S. Lidocaini. Parasti pēc procedūras nozīmīgas komplikācijas nav. Visbiežāk veidojas hematoma un zilums punkcijas vietā, var būt sāpes
b. Vakuumbiopsija – Latvijā šī krūts audu biopsijas metode netiek apmaksāta no valsts līdzekļiem, bet ir pieejama atsevišķās klīnikās. Vakuumbiopsiju veic MG vai MR kontrolē. Vakuums, kas tiek nodrošināts biopsijas laikā, neļauj punkcijas vietā izveidoties saasiņojumam.
c. Ekscīzijas biopsija – tiek veikta ļoti reti, ja nav iespējama veidojuma biopsija ar citām metodēm. Šajā gadījumā procedūra tiek veikta operāciju zālē (vispārējā vai, retāk, lokālā anestēzijā) un tiek rezecēts aizdomīgs veidojums.
Reģionālo (paduses, infraklavikulāro, suspraklavikulāro) limfmezglu tievās adatas aspirācijas (fine-needle-aspiration, FNA) citoloģiskā izmeklēšana tiek veikta, ja vizuāldiagnostiskos izmeklējumos vai palpatori rodas aizdomas par audzēja izplatību reģionālos (paduses, infraklavikulāros, supraklavikulāros) limfmezglos. Procedūru veic lokālā infiltrācijas anestēzijā ar S. Lidocaini. Parasti šo procedūru veic mammologs. Iegūto materiālu izmeklē citoloģijas laboratorijā slēdzienā atzīmējot, vai paraugā ir atrastas ļaundabīgas šūnas. Ja ir vairāki 10 aizdomīgi limfmezgli, tad citoloģijas materiālu paņem no vairākiem, īpaši, ja tie atrodas dažādās limfmezglu grupās un pusēs.
Krūts audzēja biopsijas paraugā obligāti tiek noteikti sekojoši biomarķieri ar mērķi noteikt slimības prognozi un terapijas taktiku:
Uzmanību!
Mūsdienās visām sievietēm, kam ir apstiprināta krūts vēža diagnoze, precīzi jānoskaidro HER2 stāvoklis (papildus pie atbildes 2++- FISH metode) , hormonu receptoru stāvoklis (ER un PR), dalīšanās frakcija Ki67. Ja pārbaude netiks veikta, ārsts nevarēs noteikt precīzu slimības prognozi un izvēlēties piemērotāko ārstēšanu.
· Hormonu receptoru stāvoklis: ja tiek konstatēts, ka audzēja šūnas lielā skaitā satur hormonu receptorus (estrogēna receptorus jeb ER un/vai progesterona receptorus jeb PgR), tas tiek saukts par hormonu receptoru pozitīvu – ER un vai PgR pozitīvu – audzēju. Aptuveni divām trešdaļām sieviešu krūts vēzis ir hormonu receptoru pozitīvs. Hormonu receptoru pozitīvs krūts vēzis, ļoti labi reaģē uz ārstēšanu, kas samazina hormonu daudzumu.
· Cilvēka epidermālā augšanas faktora receptora 2 (HER2) klātbūtne: HER2 ir receptors, kas atrodas uz daudzu šūnu virsmas un ir iesaistīts šūnas atbildes reakcijā uz vairāku augšanas faktoru klātbūtni. Dažu krūts vēžu šūnās ir patoloģiski liels HER2 receptoru daudzums, kas var likt šīm šūnām dalīties un vairoties daudz straujāk – tās sauc par HER2 pozitīvām šūnām. Līdz 30% krūts vēža gadījumu ir HER2 pozitīvi. HER2 pozitīvs rezultāts būtiski ietekmē krūts vēža prognozi un ārstēšanu. HER2 pozitīvs krūts vēzis ir atšķirīga slimības forma, kas prasa īpašu un neatliekamu rīcību, jo HER2 pozitīvi audzēji ir ātri augoši. Tāpēc ir būtiski, lai HER2 stāvoklis tiktu noskaidrots pēc iespējas ātrāk – tiklīdz ir atklāts krūts vēzis. Šo izmeklējumu nedrīkst atlikt līdz recidīvam vai laikam, kad slimība jau ir progresējusi. HER2 ir iespējams noteikt krūts vēža audos, kas iegūti ar kādu no biopsijas metodēm. Ja HER2 pārbaudi ārsts nav veicis biopsijas laikā, audu paraugus var uzglabāt un izmeklēt jebkurā laikā
· Ki-67 marķieri nosaka arī ar IHĶ metodi. Tas parāda, cik intensīvi audzēja šūnas dalās. Ja Ki-67 ir iekrāsojies < 10% (zems) parauga, audzējs uzskatāms par mazāk agresīvu. Ki-67 10-20% ir vidēji augsts un Ki-67 > 30% ir pārliecinoši augsts un raksturo agresīvus audzējus. Visus augstāk minētos biomarķierus parasti nosaka krūts audzēja biopsijas paraugā un operācijas materiālā neatkārto. Atbilstoši iepriekš minēto biomarķieru rezultātiem, krūts ļaundabīgus audzējus iedala četros apakštipos (skat. tabulu). Luminālam A tipam ir vislabākā prognoze, savukārt, trīskārši negatīvam krūts vēzim ir sliktāki prognostiskie izārstēšanās un dzīvildzes rādītāji. Arī terapijas taktika atsķirās atkarībā no krūts vēža apakštipa.
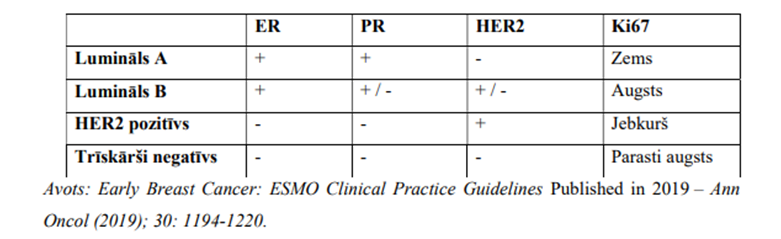
· Tāpat, krūts audu biopsijas un operācijas materiāla histoloģijā nosaka tādus audzēja parametrus kā Grade (G, diferenciācijas pakāpe), kur Grade 1 – ir vislabāk diferencēts audzējs (labāka prognoze), Grade 2 – vidēji un Grade 3 – vāji diferencēts audzējs (sliktāka prognoze).
· Nosaka arī audzēja histoloģisko tipu (pēc aktuālās WHO klasifikācijas). Visbiežākā ir sastopama duktālā karcinoma (75%), tai seko lobulāŗa (15%) un citi tipi (medullāra, papillāra, mucinoza, citi ~5%). Audzēja histoloģiskam tipam ir prognostiska nozīme.
Pārsvarā visiem audzējiem stadijas noteikšana balstās uz trim faktoriem:
audzēja izmērs un/vai audzēja izplatības laukums;
audzēja izplatība limfmezglos;
audzēja izplatība citos orgānos.
Ir vairākas krūts vēža ārstēšanas metodes. Sarunā ar ārstu tiek precizēts un pieņemts lēmums par nepieciešamo terapiju. Vērā jāņem pacienta vecums, vispārējais veselības stāvoklis un vēža stadija. Ārstēšanas veidu pēc diagnozes noteikšanas nosaka ārstu konsilijs – ķirurgs, onkologs ķīmijterapeits un radiologs terapeits (tautas valodā-staru ārsts), patologs.
Atbilstīgi ļaundabīgā audzēja lokalizācijai un stadijai var tikt izvēlēti vairāki ārstēšanas ceļi:
ķirurģiskais – operācija;
staru terapija;
medikamentozais – ķīmijterapija, hormonu terapija, mērķa terapija;
rekonstruējošā ķirurģija.
Ārstēšanu vēl var iedalīt vietējā un sistēmiskā. Vietējās ārstēšanas mērķis ir iedarboties uz audzēju, nebojājot citas ķermeņa daļas. Tādas metodes ir apstarošana un operācija.
Savukārt sistēmiskā ārstēšana nozīmē uzņemt preparātus caur kuņģa-zarnu traktu vai ievadot vēnā, tādējādi iedarbojoties uz vēža šūnām, kas ir ārpus audzēja. Pie šīm metodēm pieder hormonālā terapija, ķīmijterapija, mērķterapija un imūnterapija.
Prognoze
Prognoze ir apstākļu un rādītāju kopums, kas norāda uz izārstēšanās iespējām un terapijas izvēli.
To nosaka:
Slimības stadija - jo tā ir mazāka, jo lielākas pilnīgas izārstēšanās iespējas;
Audzēja morfoloģiskā forma un gradācija – jo audzējs ir līdzīgāks saviem veselo audu priekštečiem, jo prognoze ir labāka;
ER/PR līmenis audzēja audos. Jo tas ir lielāks, jo audzējs ar lielāku varbūtību labi reaģēs uz hormonu terapiju un būs iespējams panākt garākas slimības remisijas jeb laiku bez slimības atkārtotām izpausmēm;
HER2/neu receptoru atrade. Jo vairāk ir šo receptoru, jo audzējs ir agresīvāks un ātrāk var metastazēt. Šis rādītājs norāda uz nepieciešamību pēc mērķtiecīgas šos receptorus bloķējošas terapijas;
Vecums un blakusslimības, kas var izrādīties būtisks šķērslis sekmīgai specifiskai ārstēšanai:
Reproduktīvais stāvoklis – saglabāts menstruālais cikls vai menopauze. Menopauzē audzēji mēdz būt mazāk agresīvi un biežāk ir hormonjutīgi;
Pirmreizējs audzējs vai slimības recidīvs. Recidīva gadījumā ārstēšana parasti ir agresīvāka. Liela nozīme ir tam, cik ilgā laikā pēc sākotnējās diagnozes noteikšanas ir attīstījies slimības recidīvs. Jo šis laiks ir garāks (vairāk nekā divi gadi), jo labāka ir prognoze.
Terapijas pamatprincipi atkarībā no audzēja stadijas
Terapijas shēma, ko izvēlas paciente un viņas ārsts, būs atkarīga no slimības stadijas, audzēja izmēra, metastāzēm limfmezglos un audzēja histoloģiskajiem raksturlielumiem, kā arī sievietes vecuma, vispārējā veselības stāvokļa un blakusslimīmbām.
0 stadija
Standartterapija lielākajai daļai 0 stadijas krūts vēža gadījumu ir krūti saudzējoša operācija, kam seko staru terapija.
Alternatīva iespēja ir modificēta radikāla mastektomija (krūts un paduses limfmezglu izoperēšana) ar vai bez krūts rekonstruktīvas operācijas. Neinvazīva audzēja gadījumā papildus staru terapija nav nepieciešama.
Papildus pozitīvu receptoru gadījumā, konsīlijā izvērtēs hormonterapijas lietderību. Hormonterapija šajā gadījumā tiek nozīmēta, la mazinātu recidīvu risku.
Lobulāra karcinoma in situ ir riska faktors audzēja attīstībai tajā pašā un otrā krūtī.
Šajā stadijā svarīga ir rūpīga novērošana visā pacientes dzīves laikā (tostarp mammogrāfija ik gadu un krūts izmeklēšana reizi trīs līdz sešos mēnešos) vai pārrunājams jautājums par profilaktisku mastektomiju pacientēm, kam ģimenē ir vēža gadījumi.
I stadija
Ieteicamā terapija lielākajai daļai sieviešu ir krūti saudzējoša operācija ar veidojuma izgriešanu un paduses limfmezglu izoperēšanu, kam seko staru terapija un sistēmiska terapija.
Alternatīva iespēja ir modificēta radikāla mastektomija (krūts un paduses limfmezglu izoperēšana) ar vai bez krūts rekonstruktīvas operācijas.
Pēc operācijas, izvērtējot pacientes vispārējo stāvokli, vecumu un audzēja histoloģiskos parametrus tiek nozīmēta sistēmiskā terapija: hormonterapija, ķīmijterapija, mērķterapija.
II stadija
Operācija un staru terapijas izvēle vēža II stadijas gadījumā līdzinās tai, kādu izvēlas audzēja I stadijas gadījumā; izņēmums – II stadijas gadījumā pēc mastektomijas var apsvērt staru terapiju, ja audzējs ir liels vai izplatījies uz limfmezgliem. Pēc operācijas seko sistēmiska terapija: hormonterapija, ķīmijterapija un mērķterapija.
Sievietēm, kas vēlas krūti saudzējošu operāciju, bet kam audzēja izmērs ir 2-5 cm diametrā vai palielināti reģionālie limfmezgli, pirms operācijas nozīmē neoadjuvantu ķīmijterapiju. Tās mērķis ir mazināt audzēja izmēru, lai operācijas laikā vieglāk un drošāk varētu to izņemt.
Ja neoadjuvanta ķīmijterapija pietiekami mazina audzēja izmērus, veidojumu var izoperēt – tam seko staru terapija un papildu sistēmiska terapija. Ja audzējs nemazinās pietiekami, lai veikt krūti saglabājošu operāciju, operācijas apjoms ir mastektomija, kam seko staru terapija un papildu sistēmiskā terapija.
III stadija
Parasti ārstēšanu sāk ar pirmsoperācijas ķīmijterapiju, retos gadījumos ar hormonterapiju- atkarībā no audzēja morfoloģijas. Pēc sistēmiskas terapijas tiek veikta operācija, tad staru terapija.
PIEBILDE- Ja audzējs ir HER2 pozitīvs, tad pie neoadjuvatas ķīmijterapijas PARASTI pievieno mērķterapiju, vai gadījumos, kad pēc sistēmiskas terapijas saņemšanas krūtī un/vai limfmezglos ir reziduāla slimība (ja audzējs joprojām tiek konstatēs krūts audos vai l/m). Pirms medikamentu nozīmēšanas, ārsts lik pārbaudīt Jūsu sirdi- tiek veikts EhoKG.
Mūsdienās plaši tiek pielietota ģenētiska testēšana, arī krūts vēža gadījumā- pieejami vairāki testi
Piemēram ‘’Oncotype’’- speciāls tests, kas paredzēts gēnu analizēšanai agrīnas stadijas (audzēja izmērs līdz 5 cm, paduses metastātisko limfmezglu skaits no 1-3) estrogēnu pozitīvam, HER2 negatīvam krūts vēzim, lai noteiktu krūts vēža uzvedību un reakciju uz ķīmijterapiju. Ārsts un pacients saņem 2 atbildes- vai būs labums no plānotās ķīmijterapijas, vai tas uzlabos dzīvildzi, bezrecidīva periodu un prognozēs metastazēšanās iespēju. Tests palīdz pieņemt apzinātāku lēmumu par to vai ķīmijterapija nepieciešama.
Šo informāciju sniedz Breastcancer.org.
IV stadija
IV stadijas krūts vēza pacienšu ārstēšana ir vērsta uz audzēja masas mazināšanu, augšanas palēnināšanu, pacientes dzīves garuma palielināšanu un audzēja radīto sūdzību mazināšanu.
Pamatterapija ir sistēmiska, lietojot ķīmijterapiju vai hormonterapiju. Reizēm papildus ir nepieciešams pielietot paliatīvu staru terapiju vai retāk operāciju. Simptomātiskās terapijas veids atkarīgs no audzēja metastāžu vietas. Piemēram, sāpes kaulu metastāžu dēļ var ārstēt ar bifosfonātiem un/vai staru terapiju.
Simptomātiska terapija
Atsevišķos gadījumos slimības izplatības dēļ un pacientes vispārēji smagā stāvokļa dēļ specifisku terapiju pielietot nav iespējams. Šajos gadījumos terapijas pamatmērķis ir slimības simptomu mazināšana un vispārējā stāvokļa atvieglošana. Ārstēšana notiek sadarbojoties ģimenes ārstam un paliatīvās aprūpes speciālistam.
Lielākajai daļai sieviešu primārā audzēja ārstēšanai tiek izvēlēta operatīva iejaukšanās. Operācijas mērķis ir audzēja maksimāla izgriešana. Pirms operācijas, izvērtējot audzēja stadiju un iespējas veikt krūts saglabājošu operāciju, tiek apspriests operācijas apjoms ar ārstējošo ķirurgu. Operācijas apjoms ir atkarīgs no audzēja lieluma, lokalizācijas krūtī, pacientes krūts lieluma un izvēles saglabāt krūti.
Atkarībā no audzēja lokālas un reģionālas izplatības, ir iespējami dažādi krūts un reģionālo limfmezglu operāciju veidi. Krūšu operācijas rezultāti ir atkarīgi no pacienta faktoriem – smēķēšana, adipozitāte ir saistīti ar sliktākiem dzīšanas procesiem.
Krūts vēza operācijas nosacīti iedala divās lielās grupās:
· Krūti saglabājoša operācija, jeb sektorāla ekscīzija, tiek veikta pacientēm ar agrīnu, retāk lokāli izplatītu krūts vēzi. Operācijas laikā izņem audzēju, atstājot pārējo krūts dziedzeri. Operācija tiek veikta vispārējā anestēzijā Šobrīd krūti saglabājošu operāciju ir iespējams veikt 2 no 3 pacientēm ar krūts audzēju. Dažām pacientēm pirms operācijas tiek piedāvāta ķīmijterapija (tiek dēvēta par neoadjuvantu). Tās mērķis ir panākt audzēja un / vai tā skarto limfmezglu samazināšanos, lai būtu iespējams veikt potenciāli krūti saglabājošu operāciju.
· Mastektomija jeb visas krūts dziedzera noņemšana, tiek veikta augsta riska krūts audzēju gadījumā vai lielu audzēju gadījumā. Ir krūtsgalu (a) saglabājoša un (b) nesaglabājoša mastektomija. Pēc šādas operācijas vērojama krūšu asimetrija, ko var atrisināt ar rekonstrukciju (skat. tālāk). Pēc mastektomijas krūts āda un paduses rajons bieži paliek nejūtīgs, jutība var atjaunoties daļēji, vai neatjaunoties. (c) Profilaktisku mastektomiju veic sievietēm ar zināmu BRCA1 gēna mutāciju, lai samazinātu krūts vēža attīstības risku. Ir zināms, ka sievietēm ar pozitīvu BRCA1 gēna mutāciju ir līdz 90% risks, ka dzīves laikā attīstīsies krūts vēzis. Profilaktiska mastektomija ir abpusēja, krūtsgalu saglabājoša.
· Pēc mastektomijas ir iespējama abpusēja krūts dziedzeru rekonstrukcija ar implantiem. Latvijā šādas operācijas tiek veiktas aizvien biežāk, jo plašāk pielieto ģenētisko mutāciju noteikšanu. Profilaktiskas mastektomijas alternatīva ir ikgadējas krūts dziedzeru pārbaudes. Krūts dziedzera rekonstrukcija- tā ir operācija, kas palīdz mazināt vai pilnībā novērst asimetriju pēc krūts operācijas. Biežāk rekonstrukcijas veic pēc mastektomijas, jo pēc sektorālās rezekcijas asimetrija ir maz pamanāma. Par krūts rekonstrukcijas iespējām pacientus konsultē mammologs un plastikas ķirurgs pirms plānotas operācijas. Pirms operācijas izvēlas arī rekonstrukcijas veidu – implants vai espanders, vai arī tauku transplantācija. Implanta ievietošana var būt tūlītēja operācijas laikā vai atlikta. Visbiežāk atliktu implanta ievietošanu izvēlas, ja operācijas laikā nav iespējams ievietot tādu implanta izmēru, kas būtu simetrisks otrai krūtij. Tādos gadījumos ievieto espanderu, kuru vairāku mēnešu laikā pakapeniski piepilda ar sķidrumu. Tādā veidā pakāpeniski iestiepj ādu, rodas iespēja operētā pusē ievietot lielāku implantu un panākt simetrisku rezultātu. Dažkārt tiek veikta veselās krūts samazinoša operācija vai augmentācija ar implantu, ja nepieciešams panākt simetriju vai paciente vēlas palielināt krūšu apjomu. Krūšu rekonstrukcija pagaidām Latvijā netiek apmaksāta no valsts līdzekļiem, tomēr pacientu skaits, kas vēlas rekonstrukciju, arvien pieaug. Krūšu rekonstrukciju var veikt audzēja operācijas laikā, tā ir tūlītēja rekonstrukcija. Var izvēlēties arī novēlotu rekonstrukciju. Relatīvas kontrindikācijas krūšu rekonstrukcijai Ir smēķēšana un adipozitāte!
· Sargmezgla biopsija tiek veikta, ja pacientei vizuālgdiagnostikas izmeklējumos nav atrastas pārmaiņas limfmezglos vai arī, ja limfmezgla citoloģijā (FNA) vēža šūnas neatrod. Pirms operācijas veic limfātiskas sistēmas scintigrāfiju ar specifisku radioaktīvu vielu, kas uzskrājas pašos pirmajos limfmezglos, kuri savāc limfu no ļaundabīga krūts dziedzera audzēja. Šajos “sargājošos limfmezglos” audzējs parasti izplatās visagrāk. Parasti sargmezgla biopsiju veic vienlaicīgi ar krūts veidojuma rezekciju. Tomēr, ir gadījumi, kad sākotnēji biopsijas materiālā ir labdabīgas pārmaiņas. Tiek veikta tikai veidojuma rezekcija. Ja operācijas materiāla histoloģijā atklāj neinvazīvu (DCIS) vai invazīvu krūts vēzi, pacientiem sargmezgla biopsiju veic pēc jau veiktas sektorālās rezekcijas. Operācijas laikā caur mazu iegriezienu padusē ķirurgs ar speciālo detektoru nosaka šos sargmezglus, jo tie ir uzkrājuši radioaktīvo vielu. Sargmezgli tiek izoperēti un nosūtīti histoloģiskai izmeklēšanai. Ja sargmezglu operācijas materiālā atrod ļaundabīgas šūnas, tad var izšķirties par nepieciešamību veikt paduses limfadenektomiju (skat.tālāk). Pēc sargmezglu rezekcijas padusē var uzkrāties šķidrums, kurš periodiski ar punkcijas palīdzību ir jāevakuē. To dara mammologs. Ar laiku šķidrums pārstāj uzkrāties.
· Paduses limfadenektomija tiek veikta, kad paduses limfmezglos ir konstatētas ļaundabīgas šūnas citoloģiski un klīniski (T2-3 N1-3 M0 stadijās), un tad, ja pirms preoperatīvās terapijas limfmezglos konstatētas ļaundabīgas šūnas nereaģē uz preoperatīvu ķīmijterapiju. Limfadenektomiju parasti veic vienlaikus ar krūts audzēja operāciju. Atsevišķos gadījumos: neizdevās sargmezgla biopsija; rezecētos sargmezglos ir izteikts metastātisks process; primārs audzējs ir liels (>T2); sargmezglos saglabājas ļaundabīgas šūnas pēc preoperatīvas ķimitjerapijas u.c. - paduses limfadenektomiju veic pēc krūts operācijas. To izlemj onkokonsīlijā. Operācijas materiālu nosūta histoloģiskai izmeklēšanai. Paduses limfadenektomija ir operācija, pēc kuras var attīstīties virkne komplikāciju. Galvenā komplikācija ir rokas limfātiska tūska (limfedēma), jo pēc limfadenektomijas iztrūkst limfmezgli, kas savāc limfu no augšējās ekstremitātes. Limfedēmas profilaksei un ārstēšanai pacientiem rekomendē fizioprocedūras un limfātisko drenāžu, kā arī ir jāierobežo rokas noslogojums. Cita komplikācija pēc paduses limfadenektomijas ir šķidruma kolekcija operācijas vietā. Kolekcijas periodiski var būt nepieciešams ar punkcijas palīdzību evakuēt. To dara ķirurgs.
Staru terapija ir ārstēšanas metode, kad uz audzēja šūnām iedarbojas un iznīcina ar jonizējošu starojumu. Nepieciešamību piemērot šo terapijas veidu izvērtē konsīlija veidā.
· Latvijā staru terapiju veic P. Stradiņa KUS Onkoloģijas klīnikā, RAKUS LOC, Daugavpils reģionālā slimnīcā un Liepājas reģionālā slimnīcā
· Staru terapiju plāno un uzrauga staru terapeits, plāno medicīnas fiziķi un ikdienā ar pacientu strādā radiogrāferi
· Staru terapijas laikā katrai pacientei tiek izstrādāts individuāls terapijas plāns, aprēķināta plānotā starojuma summārā deva, atzīmēti starošanas lauki. Starojuma deva tiek sadalīta nelielu frakciju (starojuma devu) veidā, kuru paciente standartā saņem vidēji 5-6 nedēļu laikā.
· Staru terapijas laikā var rasties blakusorgānu bojājums – staru pulmonīts, sirds muskuļa bojājums, augstāk lokalizētiem audzējiem un pēc mastektomijas ir barības vada apdeguma risks. Lai minimizētu bojājuma risku, jonizējoša starojuma pievade tiek precīzi plānota, ja iespējams, pielieto elpošanas sinhronizētu staru terapiju
· Pirms staru terapijas uzsākšanas staru terapeits pacientiem sniedz informāciju par profilakses pasākumiem. Ādas apdeguma profilaksei rekomendē aizsargājošos krēmus (piem. Bepanthen), pēc dažām nedēļām, kad rodās apdegums, lokāli āda ik dienu ir jāapstrādā ar dzīšanu veicinošiem līdzekļiem (piem., Panthenol putas) līdz staru terapijas kursa beigām un vairākas nedēļas pēc tam. Plaušu bojājuma profilaksei rekomendē elpošanas vingrinājumus, sirds bojājuma profilaksei var rekomendēt Mildronāta lietošanu visas staru terapijas laikā. Svaiga gaisa ekspozīcija – pastaigas vismaz 2 st dienā, ir ļoti svarīgs profilakses pasākums, kas veicina audu dzīšanu un kardiorespiratoras sistēmas orgānu veselību. Ja rodas nopietnākas saru terapijas komplikācijas, tās arstē staru terapeits.
Staru terapija tiek nozīmēta:
Pēc krūti saglabājošam operācijām – staru terapija tiek rekomendēta visām pacientēm; staru terapija tiek veikta audzēja skartam krūts dziedzerim ar/bez papildus devas audzēja ložai.
Atsevišķām pacientēm ar zema riska audzējiem (T1a-1b, hormonpozitīvs, > 60 g.v.) var piedāvāt īso staru terapijas kursu ar lielākam reizes devām (Accelerated Partial Body Irradiation, APBI)., kur staru terapiju pievada tikai audzēja ložai 2 reizes dienā 5 dienas pēc kārtas
Adjuvantu staru terapiju var neveikt, ja invazīvs audzējs izoperēts veselu audu robežās (R0), pecientei > 70 gadi, audzējs T1N0, un paciente piekrīt 5 gadus pēc kārtas lietot hormonterapiju. Reģionālo limfmezglu (paduses, supra- un infraklavikularo, intramammāro) apstarošana ir indicēta tad, ja ir aizdomas vai dati par metastāzem attiecīgajos limfmezglos, pretējā gadījumā reģionālos limfmezglus neapstaro.
Pēc mastektomijas operācijas tā tiek rekomendēta pacientēm ar lielu audzēju un gadījumos, kad atrasta tā izplatība limfmezglos; Pēc mastektomijas staru terapija tiek pievadīta krūškurvja sienai, mastektomijas rētai un reģionāliem limfmezgliem skartā pusē atkarībā no audzēja lokalizācijas, lieluma un paduses lifmezglu statusa. Adjuvanto staru terapiju var izšķirties neveikt, ja audzējs ir zema riska, ≤ 5 21 cm, rezekcijas līnijas negatīvas, limfmezgli nav skarti (N0). Staru terapija paduses limfmezgliem +/- supraklavikulāriem un infraklavikulāriem limfmezgliem audzēja skartā pusē tiek pievadīta, ja ir atrasti metastātiski limfmezgli un tie nav pilnībā izoperēti.
Pēc neoadjuvantās (pirmsoperācijas )ķīmijterapijas un mastektomijas apstarošana indicēta tad, ja pirms neoadjuvantas terapijas bija N+ slimība, vēža šūnas ir atrastas rezekcijas līnijās (R+) vai sākotnējais audzējs bijis liels (T3N0).
Paduses limfmezglu apstarošana rada risku uz augšējās ekstremitātes limfostāzi, tāpēc tiek nozīmēta tikai pie stingrām indikācijām.
Pirms operācijas staru terapiju (neoadjuvantu) var izmantot pacientēm ar liela izmēra audzējiem, lai panāktu audzēja sarukšanu vai atvieglotu operatīvu izgriešanu;
Staru terapiju var izmantot arī kā galveno ārstēšanas veidu neoperējamas slimības gadījumā vai tad, ja paciente atsakās no operācijas;
Staru terapiju izmanto arī metastāžu izraisīto sāpju ārstēšanai, piemēram, kaulu metastāžu gadījumā.
Sistēmiskā terapija
Sistēmisko terapiju var iedalīt trīs galvenajās grupās:
neoadjuvanta – terapija, kas tiek īstenota pirms operācijas ar mērķi samazināt audzēju un / vai reģionālos limfmezglus;
adjuvanta – terapija, kas tiek piemērota atkarībā no stadijas un audzēju raksturojošiem parametriem pēc operācijas;
paliatīva – terapija, kuras nolūks ir samazināt audzēja šūnu daudzumu organismā, palēnināt to augšanu, gadījumos, kad citi radikāli ārstēšanas veidi nav iespējami
Terapijas izvēle, kā minēts iepriekš ir atkarīga gan no pacientes vispārējā stāvokļa, blakusslimībām, gan audzēja stadijas un histoloģiskajiem parametriem.
Neoadjuvanta terapija
Neoadjuvanta (pirmsoperācijas) sistēmiska terapija tiek veikta ar citotoksiskiem, mērķterapijas vai, retāk, endokrīnās terapijas preparātiem pirms potenciālas audzēju likvidējošas operācijas, retāk staru terapijas. Terapiju nozīmē un uzrauga onkologs-ķīmijterapeits.
Neoadjuvantu sistēmisku terapiju izvēlas pacientiem ar:
· krūts vēža inflamatoro formu;
· ja audzēju sākotnēji nevar radikāli (totāli) izoperēt dēļ tā lokālas vai reģionālas izplatības, t.i. IIIA (izņemot T3N1M0), IIIB, IIIC stadija;
· pacients vēlas krūti saglabājošo operāciju, bet sākotnēji audzēja izmēri tādu operāciju nepieļauj.
Neoadjuvanta terapija ir jāuzsāk 2-4 nedēļas pēc krūts vēža diagnoses apstiprinājuma. Neoadjuvantai ķīmijterapijai lieto citotoksiskus preparātus no antraciklīnu, alkilējošu un taksānu grupām, ievadot tos intravenozi. Intervāls starp kursiem (ievades reizēm) ir no 1 līdz 3 nedēļām.
Pirms katras ķīmijterapijas ievades reizes pacientiem pārbauda asins analīzes – asins ainu un bioķīmiju, vai visas asins šūnas ir atjaunojušās pēc iepriekšējā kursa, vai ir normāla aknu un nieru funkcija
Ir svarīgi laicīgi pamanīt un novērst, vai mazināt ķīmijterapijas radītos blakusefektus. Tāpēc pacienti pirms ķīmijterapijas uzsākšanas tiek informēti par iespējamiem blakusefektiem un rīcību, ja tādi rodās.
Pacienti ķīmitjerapijas laikā ir stingrā ķīmijterapeita uzaudzībā, tomēr ir būtiski, lai arī ģimenes ārsts spētu blakusefektus laicīgi pamanīt un nepieciešamības gadījumā palīdzēt pacientam.
Gadījumā, ja audzējs ir HER2 receptorus ekspresējošs, šos receptorus audzēja šūnās var bloķēt ar mērķterapiju, ievadot tos intravenozi vai zemādā. Pirms šīs grupas medikamentu nozīmēšanas ārsts obligāti izvērtē ar EHOKG palīdzību pacienta sirds funkcionālo stāvokli, jo medikaments ir kardiotoksisks. Mērķterapija ar HER2 blokatoriem, kas tika uzsākta (ar vai bez citotoksiskas ķīmitjerapijas) preoperatīvi, tiek turpināta līdz 1 gada kursam.
Pirms operācijas var nozīmēt arī endokrīno terapiju estrogēna un progesterona receptorus ekspresējošu (hormonpozitīvo) audzēju gadījumā. Neoadjuvanta hormonterapija ilgst ~3-6-9-12 mēnešus, bet ilgums var atšķirties atkarībā no terapijas panesamības un slimības dinamikas.
Pirms terapijas, terapijas laikā un pabeidzot neoadjuvantu terapiju onkologa ķīmijterapeita pienākums katras vizītes laikā ir sekot lokālajam stāvoklim, pēc nepieciešamības nozīmējot papildu izmeklējumus (US, MG, +/- MR), lai pēc iespējas ātrāk atklātu gadījumus, kad sistēmiskā terapija nav efektīva un ir nepieciešams mainīt medikamentus vai taktiku. Neefektīvas neoadjuvantās terapijas gadījumā sasaucams atkārtots multidisciplinārs konsīlijs, lai lemtu par tālāko taktiku (medikamentu maiņa, operācija, staru terapija). Pirms un pēc neoadjuvantās terapijas beigām obligāti veic vienādus krūšu izmeklējumus (parasti MRI), ar kuru palīdzību izvērtē terapijas efektu un secina par operācijas apjomu.
Adjuvanta terapija
Tā tiek dēvēta terapija, kas ir nepieciešama papildus pēc ķirurģiskas ārstēšanas. Ķīmijterapija, hormonterapija un mērķterapija tiek dēvēta par sistēmisku terapiju (preparāti nonāk asinsritē). Tās mērķis pasargāt pacienti un iedarboties uz audzēja šūnām, kas pēc operācijas iespējams ir palikušas organismā.
Adjuvantā citotoksiskā ķīmijterapija tiek nozīmēta, kad operācijas brūces ir sadzijušas. Ķīmijterapijas shēmas ir tādas pašas kādas neoadjuvantā režīmā. Terapijas nozīmēšanas un uzraudzības principi ir līdzīgi kā neoadjuvantai terapijai.
Adjuvantās ķīmitjerapijas ilgums parasti ir 3-6 mēneši atkarībā no izvēlētās shēmas. Ja pacientes veselības stāvoklis atļauj, tad atsevišķos gadījumos nozīmē tā saucamo “blīvo devu” jeb “dose-dense” ķīmijterapijas režīmu, kad ķīmijterapijas infūzijas ar standarta intervālu 3 nedēļas tiek ievadītas ik 2 nedēļas.
Adjuvantā mērķterapija tiek pielietota pacientiem ar HER2 receptoru pozitīvu krūts audzēju. HER2 receptoru blokatorus ievada monoterapijā, kopā ar adjuvanto citotoksisko ķīmijterapiju vai pēc tās. Terapijas ilgums ir 18 ievades ik 3 nedēļas, apmēram 1 gadu.
Hormonterapija
Hormonterapija piemērojama pacientēm, kurām audzēja šūnās atrasti pozitīvi hormonreceptori – ER, PR. Medikamenta darbības būtība ir organismā producēto hormonu darbības bloķēšana. Medikamenta izvēli ietekmē pacientes menopauzes statuss.
Krūts vēža pacientēm hormonterapija var ietvert vienu vai vairākus no minētajiem ārstēšanas veidiem:
Selektīvi estrogēnu receptoru modulatori – medikamenta darbības pamatbūtība ir organismā piesaiste pie estrogēnu receptoriem (organisma producētie hormoni, kas veicina šūnu, tai skaitā audzēja augšanu) un to darbības bloķēšana; Medikamenti bloķē estrogēna receptorus uz krūts vēža šūnām, ļaundabīgās šūnās netiek stimulēta DNS transkripcija, taču tiem ir virkne blakusefektu – karstuma viļņi, maksts izdalījumi, kāju/roku tūskas no šķidruma aiztures, samazināts libido, reti slikta dūša, svara zudums, menstruālā cikla nobīde. Retas, bet ļoti nozīmīgas blakusparādības ir dziļo vēnu tromboze (DVT) un plaušu artēriju tromboembolija (PATE), endometrija hiperplāzija un dzemdes karcinoma. Sakarā ar dzemdes vēža risku, pacientēm ir obligātas ikgadējas (ik 6 mēnešus) vizītes pie ginekologa ar ginekoloģisko USG. Tamoksifēnu var nozīmēt primārai profilaksei pacientēm ar pārmantotu krūts vēža risku, sekundārai profilaksei pēc krūts vēža operācijas (adjuvanti) un terapeitiskos nolūkos metastātiska krūts vēža gadījumā (paliatīvi). Sievietēm premenopauzē stingri rekomendējams lietot barjerkontracepciju visu Tamoksifēna lietošanas laiku. Krūts vēža pacientēm premenopauzē Tamoksifēns ir izvēles medikaments, ja vien nav kontrindikāciju tā lietošanai.
Aromatāzes inhibitori – medikamenti, kas nomāc organismā estrogēnu produkciju sievietēm pēc menopauzes. Šīs grupas preparāti darbojas bloķējot aromatāzi, fermentu, kas ir nepieciešams estrogēnu (estrona, estradiola) sintēzei. Visi šīs grupas preparāti ir tablešu formā un darbojas līdzīgi, kā arī tiem ir līdzīgs blakusefektu panelis – karstuma viļņi, locītavu/muskuļu sāpes, diskomforts vēderā, nogurums, depresija, slikta dūša, perifērā tūska, osteoporoze. Pacientēm pirms tearpijas ir ieteicams veikt osteodensitometriju, lai zinātu kāds ir kaulu blīvums. Postmenopauzālām sievietēm vai sievietēm premenopauzē, kurām ir olnīcu funkcijas supresija sakarā ar augstāku osteoporozes risku, adjuvanti kopā ar aromatāzes inhibitoriem var izšķirties par bisfosfonātu terapiju.
GRH analogi – preparāti, kas mazina estrogēnu līmeni organismā sievietēm pirms menopauzes;
Ovarektomija – olnīcu izņemšana ķirurģiskā ceļā (sievietēm pirms menopauzes, jo tā ir galvenā estrogēnu produkcijas vieta). Ķiruģiska kastrācija.
Hormonterapijas blaknes ir samērā bieži sastopamas. Tās ir atkarīgas no pielietotā medikamenta, tomēr visiem hormonterapijas preparātiem galvenās blaknes ir līdzīgas. Terapijas blaknes skaidrojamas ar medikamentu nomācošo iedarbību uz sievietes organisma veidoto hormonu produkciju vai tiek bloķēta to darbība šūnās. Līdz ar to rodas menopauzei raksturīgi simptomi – karstuma viļņi, svīšana, garastāvokļa mainīgums. Sievietēm pirms menopauzes vecumā vairs nav menstruālās asiņošanas.
Pacientiem ar neinvazīvu ER pozitīvu duktālu karcinomu (DCIS) pēc krūts saglabājošas operācijas, ja netiek veikta apstarošana, ir indicēta endokrīnā terapija.
Adjuvantas hormonterapijas ilgums ir parasti ≥ 5 gadi, ja vien neattīstās komplikācijas, kas šo terapiju neļauj turpināt. Ir pierādīts, ka vismaz 5 gadus ilga endokrīnā terpija mazina krūts vēža recidīva risku un pagarina bezrecidīva dzīvildzi. Jaunākie dati liecina, ka endokrīno terapiju varētu būt mērķtiecīgi pagarināt līdz 10 gadiem, bet tam ir zināmi riski saistībā ar osteoporozi un citiem endokrīno preparātu radītiem blakusefektiem. Ja pēc operācijas pacientei tiek nozīmēta arī ķīmitjerapija, tad endokrīno terapiju uzsāk pēc ķīmijterapijas pabeigšanas.
Hormonterapija paliatīvos nolūkos tiek lietota plaši- augstākminētos preparātus lieto kopā ar imūnterapiju vai mērķterapiju, lai uzlabotu terapijas efektu.
Tomēr kopumā jāpiebilst, ka terapijas ieguvumi ir lielāki un nozīmīgāki, nekā iespējamās blaknes.
Biežākās ķīmijterapijas blaknes un rekomendācijas to novēršanai
Blaknes ir ķīmijpreparātu toksisko darbību izpausme normālos (veselos) audos. Blakņu smagums lielā mērā ir atkarīgs no organisma individuālajām īpatnībām. Šobrīd pieejami daudzi un dažādi medikamenti ķīmijterapijas blakņu profilaksei un ārstēšanai. Noteikti pajautājiet par tiem savam ārstam.
Šķebināšana un vemšana
Šo nepatīkamo reakciju pamatā ir medikamentu kairinošā (ķīmisks kairinājums) iedarbība gan uz gremošanas orgānu gļotādu, gan vemšanas centru galvas smadzenēs, gan tā var izpausties arī kā nosacījuma reflekss, ieejot procedūru istabā un ieraugot zāļu pudelītes vai sajūtot to smaržu, ja iepriekšējās terapijas laikā jau bijusi šķebināšana (nelaba dūša) vai vemšana.
Dažādiem cilvēkiem šīs izpausmes var būtiski atšķirties. Biežāk tās novēro gados jaunākām pacientēm. Tāpat arī ne visi pretvēža medikamenti vienādi bieži izraisa šķebināšanu un vemšanu. Zināmi daži t.s. emetogēnie (vemšanu izraisoši) medikamenti, kas turpat divās trešdaļās gadījumu izraisa šķebināšanu un/vai vemšanu.
Profilaktiskos un ārstnieciskos nolūkos ar šo komplikāciju novērst, lietojot pretvemšanas līdzekļus. Noteikti pajautājiet par to savam ārstam. Tālāk sekos daži padomi, kā atvieglot un neizprovocēt šķebināšanu un/vai vemšanu ķīmijterapijas laikā:
Ēdiet lēni, bieži un mazām porcijām, priekšroku dodot maz vircotiem un remdeniem vai istabas temperatūrā esošiem ēdieniem;
starp maltītēm (nevis to laikā) daudz dzeriet vēsus nekairinošus, viegli paskābinātus šķidrumus maziem malciņiem (nesaldinātas dzidras sulas, kādu negāzētu minerālūdeni);
izvairieties no saldiem, trekniem un ceptiem ēdieniem;
dažkārt var palīdzēt sasaldētu sulas kubiciņu vai skābenu ledeņu sūkāšana;
izvairieties no kontakta ar jums netīkamām smaržām (ēdiena gatavošanas smakas, dūmi, spēcīgi parfīmi);
pēc maltītes mierīgi pasēdiet (vismaz divas stundas pēc ēšanas nevajadzētu atgulties, ja vien iespējams);
Matu izkrišana
Matu izkrišana atkarīga no izmantotiem ķīmijterapijas medikamentiem un pacientes īpatnībām . Daļai mati vienkārši kļūst plānāki, citām izkrīt pilnībā. Tomēr jāņem vērā, ka tā ir pārejoša parādība un terapiju beidzot mati ataug.
Dažkārt “jaunie” mati ir biezāki, citām pat sprogaini, vēl daļai tumšāki.
Matu izkrišana skar ne tikai galvas mataino daļu, bet arī ķermeņa, roku, kāju, padušu, skropstu, uzacu un kaunuma apmatojumu. Turklāt ne vienmēr galvas matu izkrišana norāda uz cita apmatojuma sagaidāmām pārmaiņām, un pretēji.
Pakāpeniski noskaņojiet domai par matu īslaicīgu zaudējumu – tā dēļ atteikties no terapijas nebūtu prātīgi. Vēlama būtu savlaicīga parūkas vai citas tīkamas galvassegas iegāde.
Terapijas laikā lietojiet maigus šampūnus un mīkstas matu sukas, netiniet matus uz ruļļiem un nežāvējiet ar karsta gaisa strūklu (ļaujiet matiem izžūt gaisā vai ieslēdziet žavētāju zemākās temperatūras režīmā); nekādā gadījumā nebaliniet, nekrāsojiet matus un nelieciet ķīmiskos ilgviļņus – tas tikai paātrinās matu izkrišanu.
Ļoti vēlams būtu pirms terapijas matus apgriezt pēc iespējas īsākus – tā mati ne tikai izskatīsies kuplāki, bet arī to izkrišana būs mazāk uzkrītoša.
Nespēks
Nespēka iemesli ķīmijterapijas laikā var būt vairāki. Pirmkārt, nespēku var radīt ķīmijpreparātu toksiskā iedarbība uz kaulu smadzenēm un eritrocītu skaita samazināšanās, kam seko skābekļa bads ar visām tam tipiskām izpausmēm – nespēku, ātru nogurdināmību, miegainību, elpas trūkumu.
Otrkārt, nespēku var radīt ķīmijpreparātu ietekme uz galvenajām aknām un nierēm. Treškārt, nespēku rada arī ķīmijterapijas ierosinātā šķebināšana un vemšana. Ceturtkārt, nespēku noteikti pastiprina nomāktais garastāvoklis un vēl virkne citu apstākļu.
Normalizējoties asins sastāvam un organismam pakāpeniski attīroties no ķīmjpreparātu sadales un šūnu sabrukuma produktiem, nespēks pakāpeniski pāries, un vispārējais stāvoklis pakāpeniski uzlabosies.
Taču, kamēr tas traucē, vērts ieklausīties šādos padomos:
ķīmijterapijas laikā pēc iespējas vairāk atpūtieties – ilgāk guliet (ja nepieciešams – lietojiet kādus miegu veicinošus līdzekļus) naktīs atrodiet iespēju pasnaust arī dienā; • iespēju robežās samaziniet savas ikdienas aktivitātes (mājas soli, iepirkšanos, bērnu vai mazbērnu aprūpi) – uzticiet uz laiku tās kādam citam. Ja tas nav iespējams, rūpīgi pārdomājiet, bez kādām darbībām pagaidām gluži labi varat iztikt;
Nespēku labi mazina dažādas dezintoksikācijas infūzijas. Tās varat veikt ambulatoriski vai pat mājas apstākļos, izsaucot aprūpes dienestu savā dzīves vietā.
Infekcijas
Toksiski iedarbojoties uz kaulu smadzenēm, ķīmijpreparāti traucē leikocītu veidošanās procesu (baltās asins šūnas, kas pasargā no infekcijas ierosinātajiem), pakļaujot organismu inficēšanās briesmām tiklab ar baktērijām, tā arī ar vīrusiem un sēnīšinfekcijām.
Visbiežāk iekaisuma ierosinātāji ir organisma paša mikroflora. Infekcijas ieejas vārti organismā var būt āda, gļotādas, elpceļi, urīnceļi, taisnā zarna, dzimumorgāni un arī injekciju vietas un katetri. Tādēļ, ja Jums ir samazināts leikocītu skaits, jo īpaši svarīgi ir ievērot personiskās higiēnas prasības.
Iespēju robežās izvairieties no saskarsmes ar slimiem vai nesen slimojušiem cilvēkiem.
Svarīgi ir zināt tos simptomus, kuri varētu liecināt par iespējamu infekciju un kuru gadījumā nekavējoties jāziņo savam ārstam. Tie ir:
temperatūras paaugstināšanās virs 38 grādiem,
drebuļi,
pastiprināta svīšana,
klepus vai kasīšanās sajūta kaklā, šķidra vēdera izeja,
dedzinoša sajūta urinācijas laikā;
izdalījumi no maksts vai lokāls ādas apsārtums vai satūkums, īpaši pievēršot uzmanību injekcijas vietām.
Asiņošana
Ķīmijterapijas laikā nereti kaulu smadzeņu toksiskā bojājuma dēļ vērojama trombocītu skaita samazināšanās, kā arī līdz galam nenobriedušu un līdz ar to arī funkcionāli nepilnvērtīgu trombocītu nokļūšana asins straumē. Tas savukārt var būt par iemeslu asiņošanai, kas var izpausties gan kā sīki punktveida zemādas asinsizplūdumi, pastiprināta zilumu veidošanās, sārti iekrāsojies urīns, tumši vai asiņaini izkārnījumi, kā arī lielākas vai mazākas asiņošanas epizodes no deguna, smaganām, dzimumceļiem.
Ja Jums parādās kāda no minētajām izpausmēm, noteikti ziņojiet savam ārstam. Jums pārbaudīs asinsainu un, atkarībā no trombocitopēnijas (samazināts trombocītu skaits asinīs) smaguma, noteiks attiecīgu ārstēšanu.
Gļotādu bojājumi
Gremošanas orgānus izklājošā gļotāda ir sevišķi jutīga pret ķīmijpreparātu toksisko iedarbību. Tādēļ terapijas laikā nereti novēro mutes un rīkles gļotādas iekaisumu, jēlumus, nereti – šīs gļotādas izsausē un tādējādi kļūst sevišķi viegli ievainojamas un bieži asiņo. Šie mutes un rīkles gļotādu bojājumi ir ne tikai ļoti sāpīgi, bet draud arī ar bakteriālas vai sēnīšinfekcijas pievienošanos.
Tā kā atveseļošanās parasti noris lēni, svarīgi ievērot dažus profilakses pasākumus jau no paša terapijas sākuma.
Ķīmijterapija bieži vien provocē pastiprinātu zobu bojāšanos un smaganu iekaišanu, tādēļ mērķtiecīgi vēl pirms terapijas būtu aiziet pie zobārsta un salabot esošos caurumus, kā arī pārbaudīt smaganu stāvokli un zobu protēžu atbilstību Lietojiet jutīgām smaganām paredzētās zobu pastas un ļoti mīkstu zobu suku. Izvairieties no karstu un vircotu, kā arī rupjšķiedrainu un kairinošu (skābu, sāļu) produktu lietošanas. Priekšroku terapijas laikā dodiet smalki saberztiem vai sasmalcinātiem produktiem – kartupeļu biezputrai, biezpienam, mīkstiem augļiem (banāniem), dažādiem pudiņiem, mīksti vārītām biezputrām, ķīseļiem, biezeņzupām. Lietojiet pietiekami daudz nekairinoša šķidruma – tējas, atšķaidītas sulas, ķīseļus.
Caureja
Jūsu slimības gadījumā biežākais caurejas iemesls ir tieši ķīmijterapija. Ja tās laikā vai drīz pēc pabeigšanas caureja ar vairākkārtīgu vēdera izeju turpinās ilgāk par 24 stundām, turklāt, ja to vēl pavada arī krampjveidīgas sāpes vēderā, noteikti ziņojiet par to ārstam.
Smagākos gadījumos Jums var tikt nozīmēta īpaša terapija (bez konsultācijas ar ārstu pati uz savu roku labāk neko neuzsāciet) – medikamenti vai pat šķidrumu infūzijas.
Nervu bojājums
Dažiem ķīmijpreparātiem piemīt selektīva toksiska iedarbība uz nervu šķiedrām, radot tā saucamo perifērisko neiropātiju (nervu šķiedru bojājums). Tās izpausmes var būt gan tirpšanas, durstīšanas vai salšanas sajūtas roku un kāju pirkstos, gan līdzsvara traucējumi, grūtības paņemt rokā un noturēt sīkus priekšmetus, aizpogāt apģērbu, veikt kādas precīzas manipulācijas ar pirkstiem. Dažiem pacientiem var būt stīvuma sajūta mēlē un pat rīšanas traucējumi. Citiem perifērisko nervu šķiedru bojājums var izpausties ar sāpēm žokļos, vēderā, ar dzirdes pasliktināšanos vai vēdera aizcietējumu (bojāti zarnu sieniņu motoriku nodrošinošie sīkie nerviņi). Šīs komplikācijas, lai arī nepatīkamas, vairākumā gadījumu tomēr ir pārejošas. Minētās sūdzības un tās profilakses, ārstēšanas iespējas vēlams apspriests ar ārstējošo ķīmijterapeitu. Tomēr jāņem vērā, ka perifēriskā neiropātija uzreiz neizzudīs pēc terapijas beigām un paies zināms laiks, kamēr nervu šķiedras atveseļosies.
Šo komplikāciju vislabāk var ārstēt neirologi, lietojot neiropātisko sāpju ārstēšanai paredzētos medikamentus.
Ādas un nagu bojājums
Biežākās ķīmijterapijas toksiskās izpausmes ādā ir apsārtums, nieze, ādas sausums, lobīšanās. Savukārt nagi mēdz kļūt trausli, tumši, nespīdīgi, viegli lūstoši, ar vertikālu gropējumu. Daži ķīmijpreparāti pēc intravenozas ievadīšanas var radīt ādas tumsnēšanu pa vēnas gaitu, kas parasti gan ir pārejoša parādība. Pamatots ir ieteikums izvairīties no tiešu saules staru iedarbības, jo daži medikamenti mēdz radīt īpatnēju ādas plankumainību saskarē ar ultravioletajiem stariem. Nereti pacientiem, kas iepriekš bijuši apstaroti, pēc ķīmijpreparātu ieņemšanas vai ievadīšanas starojuma vietās novēro ādas apsārtumu, ko var pavadīt sāpes, nieze vai dedzināšana. Lielākoties ādas bojājumi nav smagi un īpaša ārstēšana parasti nav nepieciešama.
Taču noteikti atgādināmas tās situācijas, kad nekavējoties jāinformē medicīniskais personāls:
ja intravenozas medikamentu ievades laikā parādās asas sāpes, dedzināšana vai citāda nepatīkama kairinoša sajūta injekcijas vietā;
pēkšņa vispārēja nieze, izsitumi pa visu ķermeni vai ādas plaisājumi, jo īpaši, ja tos vēl pavada arī elpošanas grūtības (pēkšņi kļuvis smagi elpot), sirdsklauves, panisku baiļu sajūta.
Nieru un urīnpūšļa darbības traucējumi
Daži ķīmijpreparāti toksiski iedarbojas uz urīnpūšļa sieniņu, vēl daži var radīt īslaicīgus vai paliekošus nieru parenhīmas bojājumus. Parasti tie ir jau zināmi preparāti, un to lietošanu vienmēr kombinē ar atbilstošu aizsargterapiju – īpašiem medikamentiem vai pastiprinātu šķidruma pievadi infūziju veidā. Ārsts būtu jāinformē visos tajos gadījumos, ja ķīmijterapijas laikā parādās sāpes urinācijas laikā, urinācija kļuvusi biežāka, nereti ir spiedošas ļoti pēkšņas vajadzības un pat patvaļīga urīna noplūde, urīns kļuvis sārts, kā arī, ja Jums ir drebuļi un paaugstināta temperatūra (virs 38 grādiem).
Ķīmijterapijas laikā vēlams dzert daudz šķidruma – tas palīdzēs skalot nieres un urīnpūsli un mazinās toksisko izpausmju attīstības risku. Ja nav citādu ierobežojumu, dzert varat jebko, kas Jums garšo – ūdeni, sulas, tēju, kafiju, limonādi, buljonu, ķīseli.
Ēstgribas trūkums
Samazināta ēstgriba, tās trūkums vai pat pilnīga atteikšanās no ēdiena ir samērā biežas parādības. Iemesli ēstgribas trūkumam var būt dažādi – ķīmijterapijas blaknes (šķebināšana, vemšana, anēmija), depresija, sāpes, nogurums.
Daži ierosinājumi, kā rīkoties šādās situācijās:
ēdiet, cik bieži un kad vien vēlaties. Nesaistiet sevi ar noteiktām ēdienreizēm, bet izmantojiet katru ēstgribas parādīšanās brīdi;
ēdienu bagātīgi papildiniet ar garšvielām (bet ne asām!), īpaši aromātiskām, un, ja iespējams, ēdienu skaisti dekorējiet;
ēstgribu noteikti uzlabos neliela fiziska slodze tieši pirms maltītes; nomazgājiet seju un rokas, izvēdiniet telpas;
pacentieties nedzert pirms ēšanas;
ēdienu uz šķīvja lieciet ļoti mazām porcijām, jo liels apjoms vēl vairāk atbaidīs no ēšanas;
pirms ēšanas noteikti izskalojiet muti, iztīriet zobus un, ja moka sāpes, vismaz pusstundu pirms gaidāmās maltītes ieņemiet kādu pretsāpju līdzekli;
varat lietot kādu no tautas līdzekļiem apetītes veicināšanai (vērmeļu, apiņu uzlējums, aptiekās nopērkamās šiem mērķiem paredzētās īpašās gatavās tējas).
Seksualitāte un auglība
Pārmaiņām seksualitātē vairāk ir psiholoģisks, mazāk medikamentu pastarpināts iemesls. Ja slimība nav izjaukusi savstarpējo attiecību harmoniju (nereti tas ir lūzuma posms daudzu pāru kopdzīvē), tad arī intīmajā sfērā visticamāk nekas nemainīsies. Var gadīties, ka partnera atturību rada nevis nevēlēšanās, bet bailes Jums nodarīt pāri, izraisīt sāpes. Gadās, ka partneris, nebūdams pietiekami informēts, baidās no Jums inficēties. Te nekas nepalīdzēs labāk par atklātu sarunu.
Jaunām sievietēm ķīmijterapijas laikā var mainīties menstruālais cikls un asiņošanas intensitāte. Citām savukārt var attīstīties klimaktērijam līdzīgi simptomi – karstuma viļņi un nieze, dedzināšanas vai sausuma sajūta makstī.
Nav izslēgta ķīmijpreparātu toksiska iedarbība arī uz olnīcu audiem ar pārejošas vai paliekošas neauglības attīstība. To nosaka daudzi un dažādi apstākļi, taču šis jautājums noteikti pārrunājams ar Jūsu ārstējošo ārstu vēl pirms terapijas sākšanas.
Ja sieviete nelieto kādu no kontracepcijas līdzekļiem, pastāv iespēja, ka ķīmijterapijas laikā var iestāties grūtniecība. Visbīstamākais auglim ir tieši pirmais trimestris (pirmās 12-16 grūtniecības nedēļas), kad ķīmijpreparāti var radīt attīstības anomālijas, ja vien grūtniecība nebeidzas ar spontānu abortu. Tādēļ visām sievietēm pirms terapijas sākšanas vēlams būt skaidrībā par sevi un veikt grūtniecības pārbaudes testu.
Grūtniecība
Var gadīties, ka slimību diagnosticē brīdī, kad Jūs jau esat stāvoklī. Tālākā terapijas taktika tad būs atkarīga no grūtniecības laika, slimības stadijas, morfoloģiskās formas un daudziem citiem blakus apstākļiem. Ja būsiet grūtniecības sākumā (līdz 12. nedēļai), visticamāk, ārstu konsīlijs Jums piedāvās grūtniecības pārtraukšanu. Atsakoties no šī piedāvājuma, Jūs galvenokārt riskējat ar savu veselību, ar terapijas iekavēšanu vai nepilnīgu ārstēšanas kursu, kas var pasliktināt Jūsu slimības gaitu, turklāt augļa izredzes uz pilnvērtīgu attīstību šai gadījumā ir ļoti niecīgas. Ja slimības diagnosticēšanas brīdī esat grūtniecības vidējā trimestrī (no 13. līdz aptuveni 24.-26. nedēļai) un ja esat noteikti izlēmuši bērniņu saglabāt, iespējama ķīmijterapijas došana uz daļēji “atvieglotiem” nosacījumiem. Arī šai gadījumā augļa bojājuma risks saglabājas, taču tas ir nedaudz mazāks nekā pirmajā trimestrī. Grūtniecības trešajā trimestrī diagnosticētu audzēju gadījumā parasti vai nu nogaida dabīgo dzemdību termiņu vai to mākslīgi paātrina un tad sāk intensīvus ķīmijterapijas kursus.
Nav pierādīts, ka grūtniecība pēc veiksmīgi izārstēta krūts vēža palielinātu slimības atjaunošanās vai augļa anomāliju risku. Noteikti vēlama izsargāšanās pirmos 3–5 gadus pēc pabeigtas ķīmijterapijas. Tas nepieciešams, jo vairākumā gadījumu slimības recidīvs attīstās tieši šajā laikā. Ja būsiet to veiksmīgi pārdzīvojusi, Jūsu izredzes uz izārstēšanos ir lielākas, un varat plānot arī grūtniecību. Protams, tas prasīs detalizētu sarunu ar ārstu par visiem iespējamiem riskiem un to novēršanu. Terapijas laikā un vēlams arī turpmākos 3-5 gadus vajadzētu lietot drošu kontracepciju. Ja vairs neplānojat bērnu radīšanu, visdrošākā metode ir sterilizācija. Pārējās kontracepcijas metodes jāapspriež ar ginekologu un onkologu.
Limfostāze
Limfostāze – limfas atteces traucējumi operētajā pusē, kas izpaužas ar tūsku. Ja pavairotais limfas daudzums nespēj drenēties, tas sāk uzkrāties audos – taukaudos, ādā, muskuļos, saistaudos, nervu audos un asinsvados, tos nospiežot un radot attiecīgās sūdzības kā smaguma sajūtu, sāpes, pastiprinātu nogurumu rokas un plecu daļā, rokas apjoma pieaugumu vai ādas krāsas pārmaiņas.
Procesa attīstības mehānisms ir - operācijas vai apstarošanas rezultātā limfātisko drenāžas kapilāru tīkls ir samazināts vai neatgriezeniski pārrauts, tiek apgrūtināta novadīšana no audiem. Limfostāzes risks palielinās situācijās, kad palielinās apasiņošana rokā (iekaisums, apdegums, muskuļu pārslodze, kukaiņu kodums, traumas). Tādēļ turpmāk slimās puses roka ir jāsaudzē.
Limfostāze var skart visu roku vai tikai daļu no tās – plaukstu, apakšdelmu, elkoņa apvidu. Nereti limfostāze var veidoties krūts apvidū, jo arī šīs anatomiskās vietas limfa drenējas caur paduses limfmezgliem.
Limfostāzi pēc krūts operācijas dažādās smaguma pakāpēs novēro 5-40% gadījumu. Sargātājlimfmezgla izoperēšana limfostāzes risku būtiski samazina līdz 3-13%, taču nenovērš to pilnībā.
Limfostāzes epizodes var ilgt no dažām dienām līdz vairākām nedēļām. Ja limfostāze saglabājas vairākus mēnešus, ar vislielāko varbūtību tā būs paliekoša.
Tomēr tikai ļoti retos gadījumos limfostāze ir galēji smaga ar būtiskiem funkcionāliem traucējumiem.
veikta paduses limfmezglu izoperēšana;
veikta gan limfmezglu izoperēšana, gan vēlāk – paduses apstarošana;
bijušas masīvas metastāzes paduses limfmezglos;
saņemta ķīmijterapija;
veikta mastektomija, nevis veidojuma izgriešana;
aptaukošanās;
smēķēšana;
diabēts;
agrāk veikta operācija paduses apvidū.
Ārstēšanā un profilaksē ir vērā ņemamas rekomendācijas no ķirurga par kustību iestrādes atsākšanu pēc operācijas, pieļaujamo slodzi un vingrojumiem pēcoperācijas periodā.
Svarīgi ievērot arī citus profilakses pasākumus:
regulāri mitriniet ādu;
turiet rokas un plaukstas tīras, nelietojiet ādas skrubjus vai sukas mazgāšanās laikā;
vienmēr lietojiet cimdus, strādājot virtuvē (pat mazgājot traukus) vai dārzā;
strādājot (beržot, tīrot, mazgājot) ieturiet biežas pauzes – atsēdieties un paceliet roku, to maigi paglaudot virzienā uz padusi;
lietojiet kukaiņu atbaidošus aerosolus, vēlams tādus, kas nesatur alkoholu;
vienmēr apziediet ādas bojājuma vai koduma vietu ar antiseptisku un/vai antibakteriālu ziedi (fucidīna ziede, streptocīda ziede, sintomicīna liniments);
obligāti lietojiet saules pretapdeguma krēmus ar aizsargskaitli vismaz 30;
šujot vienmēr lietojiet uzpirksteni;
atpūšoties atbalstiet roku paceltā stāvoklī, bet nekad neturiet roku, paceltu bez atbalsta;
ja Jums ir diabēts, sevišķi rūpējieties ne tikai par savu roku, bet arī par cukura līmeni;
pirms iekāpšanas lidmašīnā roku nosaitējiet ar kompresijas bandāžām (tikai tad, ja Jums jau ir limfostāze);
neejiet karstā dušā vai vannā, nelietojiet kontrastainas ūdens strūklas (auksts-karsts), mazgājot traukus vai dušojoties, neapmeklējiet saunas vai tvaika pirtis;
nelietojiet karstus apliekamos un kompreses attiecīgai rokai, tās pašas puses kakla un plecu apvidū; tāpat izvairieties arī no šo zonu dziļās masāžas, ultraskaņas procedūrām, citām siltuma un elektroprocedūrām;
nenesiet smagumus uz leju nostieptā rokā;
nenēsājiet kustības ierobežojošu, apspīlētu apģērbu;
juvelierizstrādājumus valkājiet uz veselās rokas;
nelietojiet smagu krūts ārējo protēzi;
neaizraujieties ar alkoholu, jo tas paplašina asinsvadus un atvieglo šķidruma izdali ārpus tiem;
nesmēķējiet, jo smēķēšana sašaurina sīkos asinsvadiņus un apgrūtina jau tā ierobežoto šķidruma plūsmu;
manikīra laikā izvairieties no kutikulu apgriešanas;
skartajā rokā centieties izvairīties no manipulācijām kā injekcijas, asinsspiediena mērīšana, vakcinācija;
izvairieties no statiskas slodzes, bērna cilāšanas, mājas ģenerāltīrīšanas, veļas gludināšanas
Fiziskās aktivitātes
Kustības un muskuļu saraušanās stimulē limfas plūsmu. Vispiemērotākā fiziskā nodarbe rokas limfostāzes profilaksei un arī stāvokļa stabilizācijai un simptomu mazināšanai ir peldēšana un ūdens aerobika. Mehāniskais ūdens spiediens no ārpuses un fiziskās kustības ļoti labvēlīgi ietekmē rokas limfātisko sistēmu.
Tāpat ieteicami dažādi lokanības un stiepšanās vingrinājumi, Pilāta (Pilates) vingrinājumi, ļoti pakāpeniski slodzes vingrinājumi ar vieglām hantelēm. Vislabāk šos jautājumus ir pārrunāt ar pieredzējušu fizioterapeitu vai ergoterapeitu.
Kompresijas bandāžas un piedurknes - pirms bandāžas saites vai piedurknes iegādes konsultējieties ar fizioterapeitu, kurš palīdzēs Jums izvēlēties pareizo izmēru un ierādīs, kā pareizi uzliekama bandāžas saite, lai tā nenospiestu roku un neradītu vēl lielākas problēmas.
Lai sāktu ārstēšanu, nepieciešams ģimenes ārsta norīkojums. Ja ir kaut nelielas aizdomas par izmaiņām krūtī, ģimenes ārstam jādod sievietei norīkojums uz kādu no specializētajām onkoloģijas ārstniecības iestādēm Rīgā, Liepājā vai Daugavpilī.
Ja nav ģimenes ārsta nosūtījuma, šajās iestādēs ir pieejami arī maksas pakalpojumi – mamogrāfija, ultrasonogrāfija un konsultācijas.